Уксусная кислота может реагировать с серебром
Опубликовано: 24.07.2024

Серебро с древних времен ценилось и считалось драгоценным металлом. Он имеет антисептические свойства, прост в обработке и проводит электричество. Большинство людей имеет дело с серебряными украшениями или столовыми приборами. Из-за окисления и загрязнения возникает необходимость в очистке, а дороговизна или «наследие» (такие вещи могут храниться много поколений) порождают излишнюю осторожность при выборе методов и средств.
Можно ли чистить серебро уксусом
Чистое серебро не вступает в реакцию с кислотами. Это значит, что такая обработка избавит предмет от всего, кроме самого металла.
Однако в этом процессе есть свои тонкости, например, уксус запрещено использовать в след. случаях:
- Сплав серебра и других металлов. К таким исключениям можно отнести и напыление на поверхности изделия. В современных столовых приборах и (особенно) украшениях серебро часто имеет покрытие из родия для большей устойчивости к окислению и повреждениям. Но если покрытие из дешевого металла – кислота может вступить в реакцию.
- Инкрустированные драгоценные камни. Чистка украшений сильными веществами чревато помутнением или повреждением камней. Такие изделия крайне желательно чистить вручную без использования привычных бытовых веществ.
- Состав уксуса. Бытовой вариант – это сильно разбавленная версия кислоты. Некоторые виды такого уксуса содержат пищевые добавки, которые могут вызвать проблемы: неестественно долгую реакцию или смену окраса. Стандартная версия (9%) подойдет для чистки, но стоит обращать внимание на состав: доля уксусной кислоты и наличие красителей.
Реакция серебра на кислоту
При использовании уксуса происходит его взаимодействие с оксидами и прочей грязью, что накопилась в изделии. Однако само серебро (как и ряд других металлов) не вступает в реакцию с кислотами.
Эту особенность используют для проверки серебра на подлинность.
Уксус избавит от большинства видов налета. Скорость очистки зависит не только от уровня загрязнения, но и от его происхождения, а также вида. Нежелательное покрытие появляется из-за:
- Пота: если украшение контактирует с телом (крестик, браслет, ожерелье).
- Косметики: актуально для украшений.
- Еды: проблема столовых приборов.
- Особенностей хранения: касается помещений с высокой влажностью или банальным отсутствием должного ухода за предметом.
- Сплав: наличие другого металла, который по-своему окисляется и реагирует на окружающую среду. Кроме серебра, «иммунитет» к кислотам имеют такие металлы как медь, золото, платина и ртуть. Но если на изделии, например, напыление из никеля – кислота (в данном случае – уксус) войдет в реакцию, образуя соль, и уничтожая напыление.
Поэтому, если серебро низкой пробы, или это сплав с металлом, реагирующим на серебро, то лучше чистить его, не прибегая к кислотам.
Как правильно чистить серебро уксусом: советы

Чтобы избавиться от налета с помощью уксуса без дополнительных химикатов, понадобятся:
- кастрюля или котел: после процесса эта емкость будет непригодной для кулинарии;
- средства защиты – респиратор и перчатки;
- щипцы;
- уксусный раствор. Его создают из белого уксуса и соли с дистиллированной водой (обычная вода содержит определенную долю веществ, которые могут все испортить). Соль добавить в расчете 1 столовая ложка на стакан воды. В эту воду залить уксус (но не наоборот).
- Тщательно протереть серебряное изделие от пыли и жира.
- Залить раствор в кастрюлю и нагревать почти до кипения. Высокая температура ускорит реакцию.
- Поместить туда загрязненные украшения/приборы.
- Подождать, пока налет и оксиды не исчезнут. Время ожидания зависит от уровня загрязнения и количества уксуса в чистящей жидкости.
- Извлечь серебряные изделия щипцами, тщательно промыть их и протереть сухой и чистой тряпкой.
Такой метод актуален для особо запущенных случаев. Суть действий особо не изменится, если чистящее средство будет не самодельным, а покупным. Но последнем случае лучше ориентироваться на инструкцию.
Чистка серебра содой и уксусом: пошагово
Сода понадобится, когда проявились более очевидные проблемы.
Разведение уксуса. Для этого метода нужна емкость (она не станет одноразовой) и сам уксус. После очистки от обычной грязи серебро нужно поместить в уксус: он должен доходить до краев изделий. Ожидание может длиться от 15 минут до нескольких часов. Затем изделия нужно извлечь, промыть и насухо вытереть.
Добавлять соду следует в количестве 1 ст. л на стакан воды. В таком случае короткое ожидание бессмысленно, и извлекать серебро можно будет примерно через три часа.
Важно и то, что сода может использоваться как самостоятельное чистящее средство. В таком случае ее смешивают с водой в таких пропорциях, чтобы получилась субстанция вроде каши, которую наносят на чистящую поверхность или ткань и обрабатывают загрязненное изделие.
Выводы

Реакция серебра на кислоту под действием высокой температуры (на мини печи)
Благодаря стойкости к кислотам серебро можно чистить обычным уксусом. Это актуально и для других кислот, таких как лимонная: из-за повышенной концентрации её часто применяют в случаях высокого загрязнения.
Если сильнодействующие кислоты не подходят – можно использовать нашатырь, оливковое масло или зубной порошок.
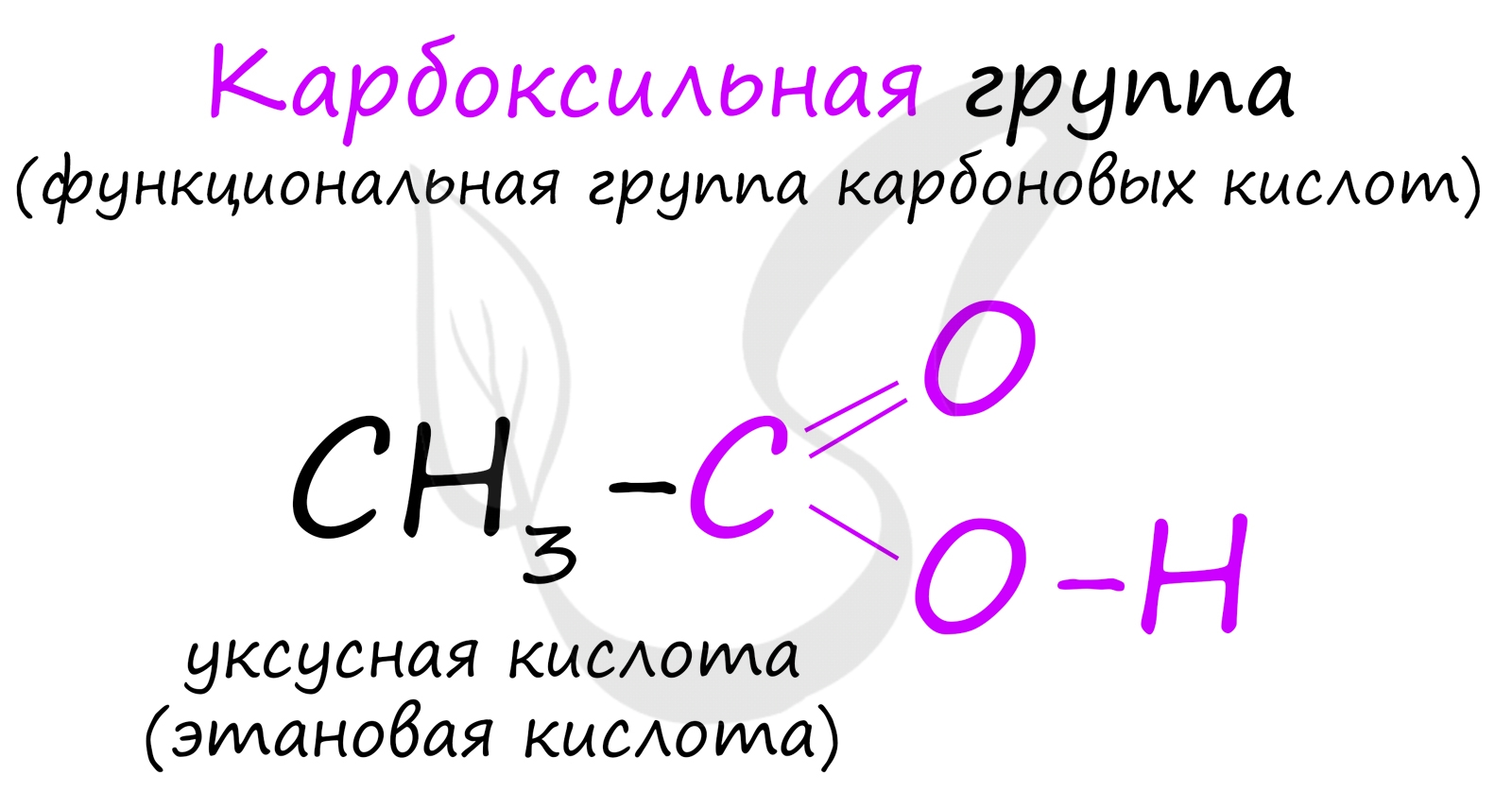
Карбоновые кислоты - класс органических соединений, молекулы которых содержат одну или несколько карбоксильных групп COOH.
Имеют разнообразное промышленное применение и большое биологическое значение. Общая формула одноосновных карбоновых кислот CnH2nO2 .
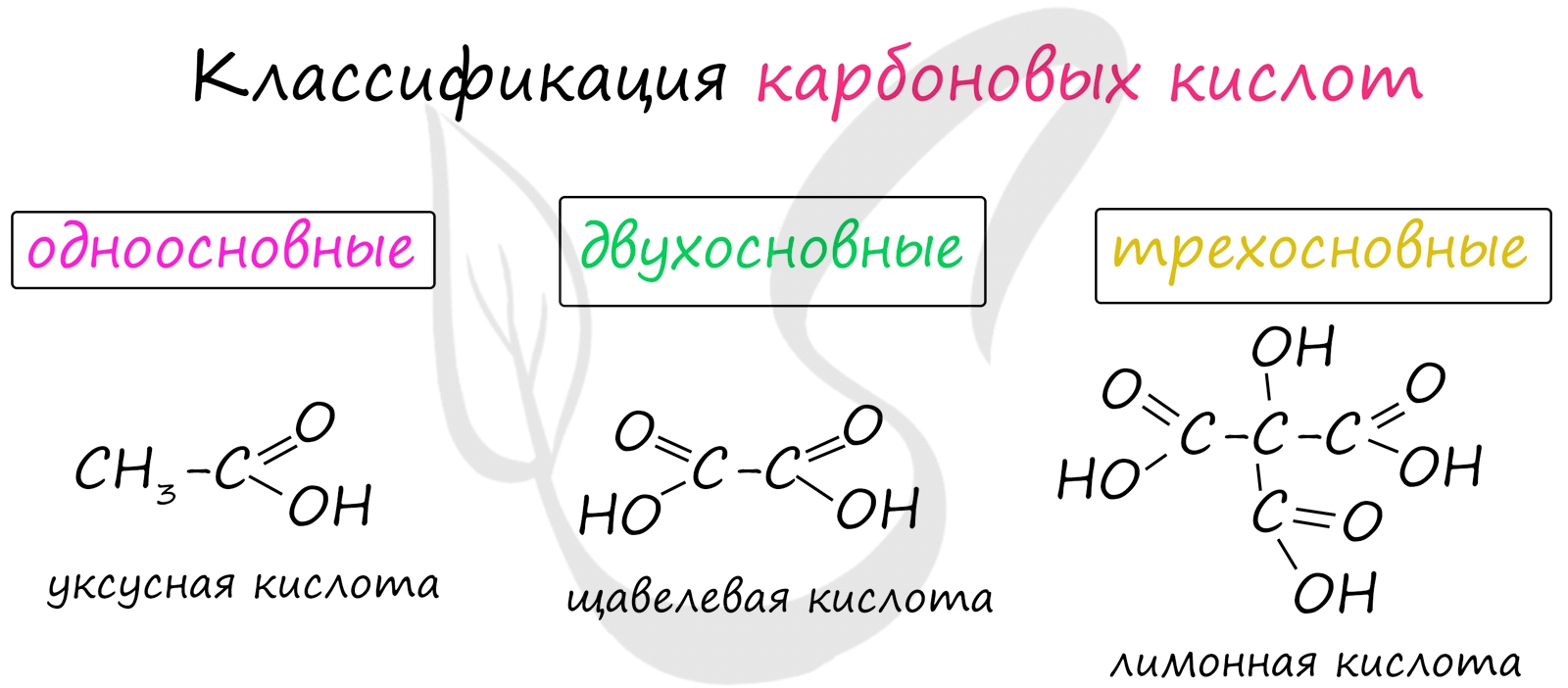
Классификация карбоновых кислот
По количеству карбоксильных групп в молекуле карбоновые кислоты подразделяются на:
- Одноосновные - 1 карбоксильная группа
- Двухосновные - 2 карбоксильных группы
- Трехосновные - 3 карбоксильных группы
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
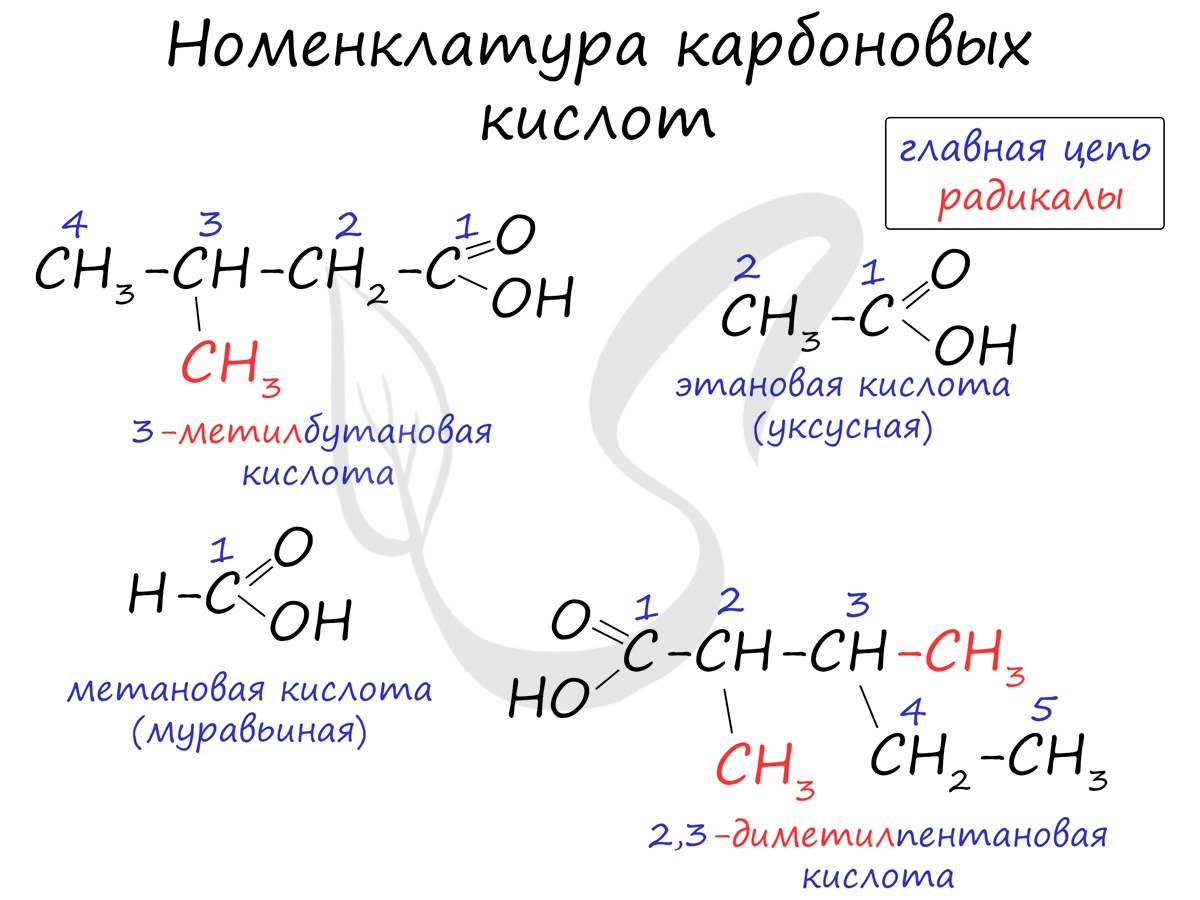
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса "овая" к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
Многие карбоновые кислоты имеют тривиальные названия. Наиболее известные:
- Метановая - HCOOH - муравьиная кислота
- Этановая - CH3-COOH - уксусная кислота
- Пропановая - C2H5-COOH - пропионовая кислота
- Бутановая - C3H7-COOH - масляная кислота
- Пентановая - C4H9-COOH - валериановая кислота
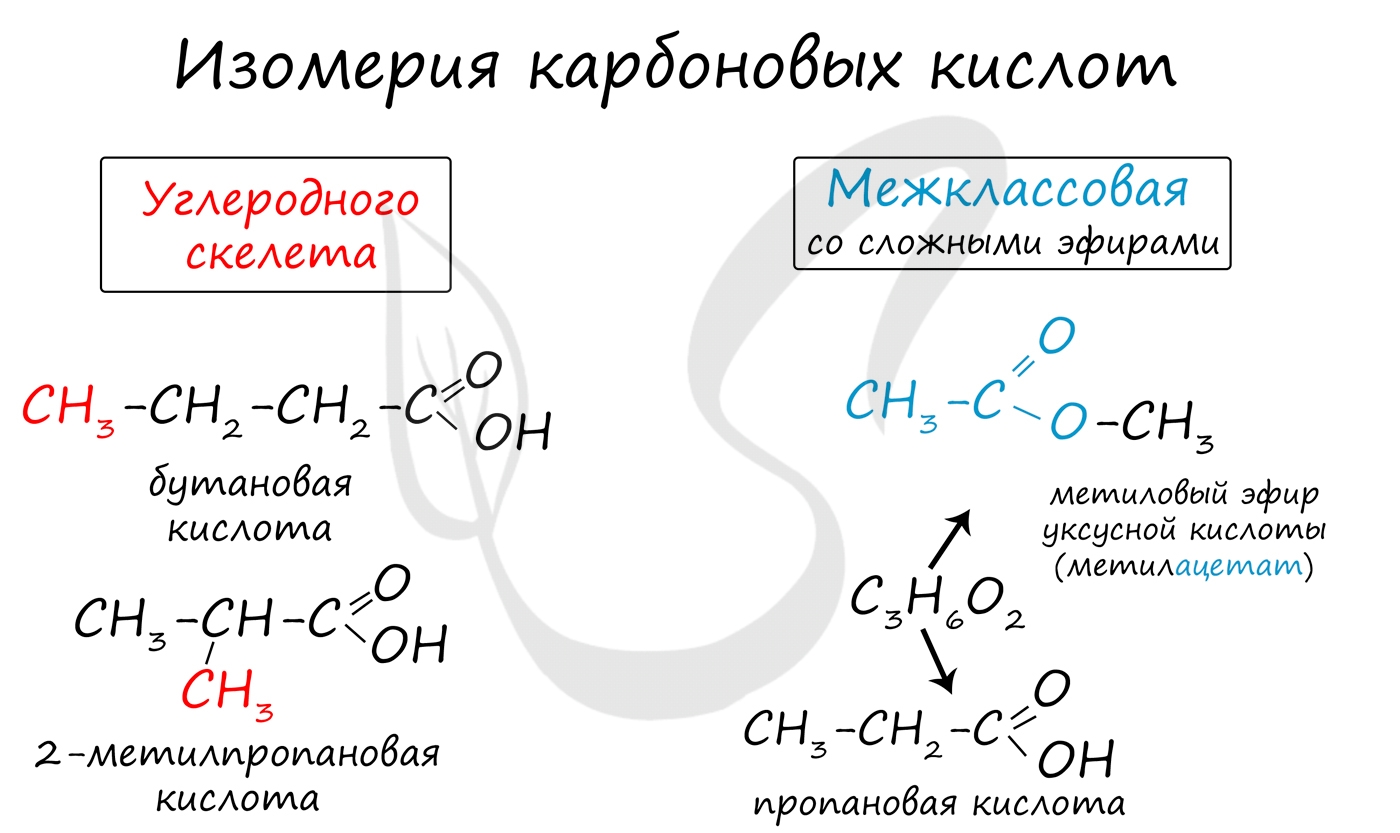
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
- Окисление алканов
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
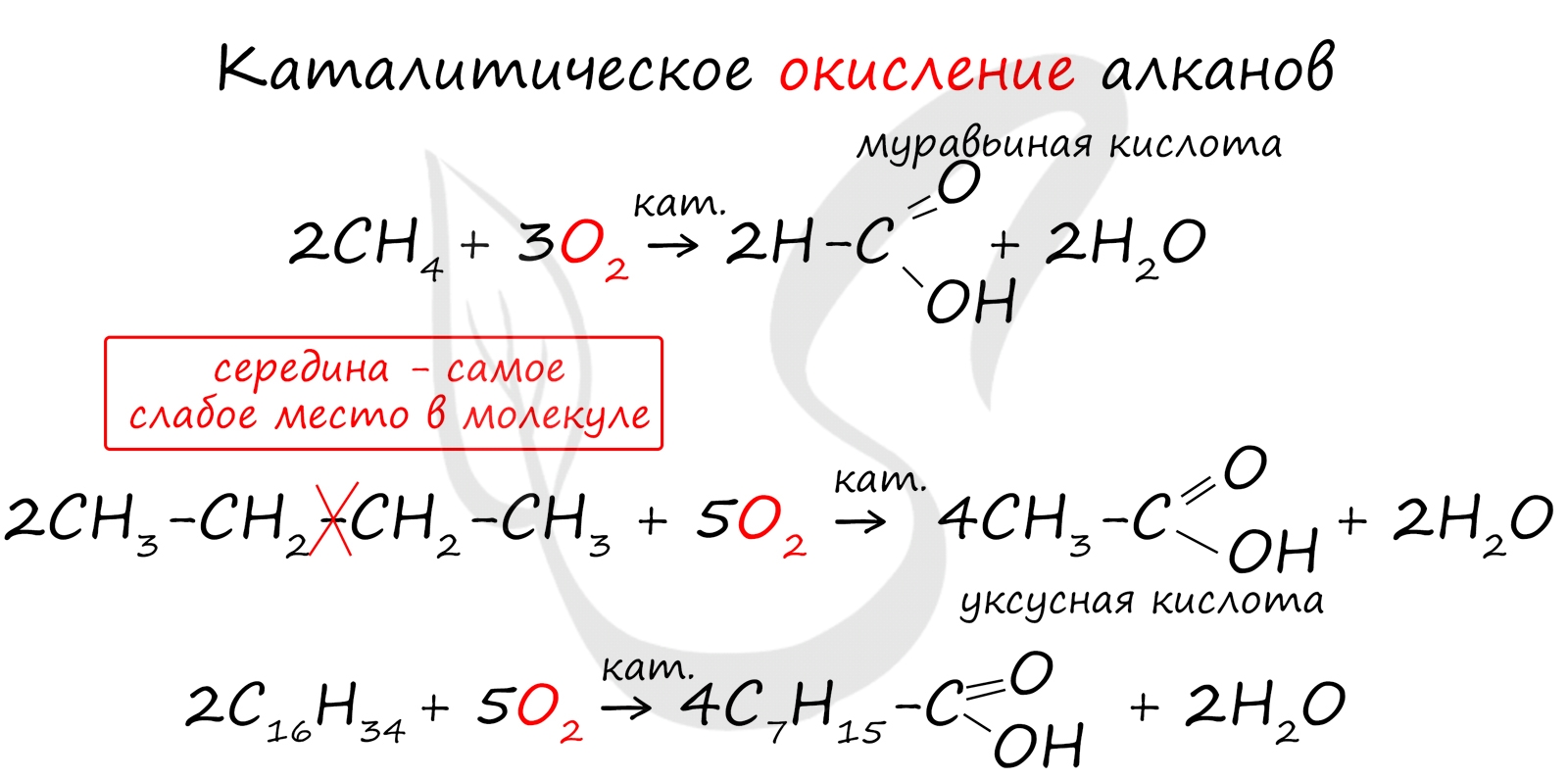
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
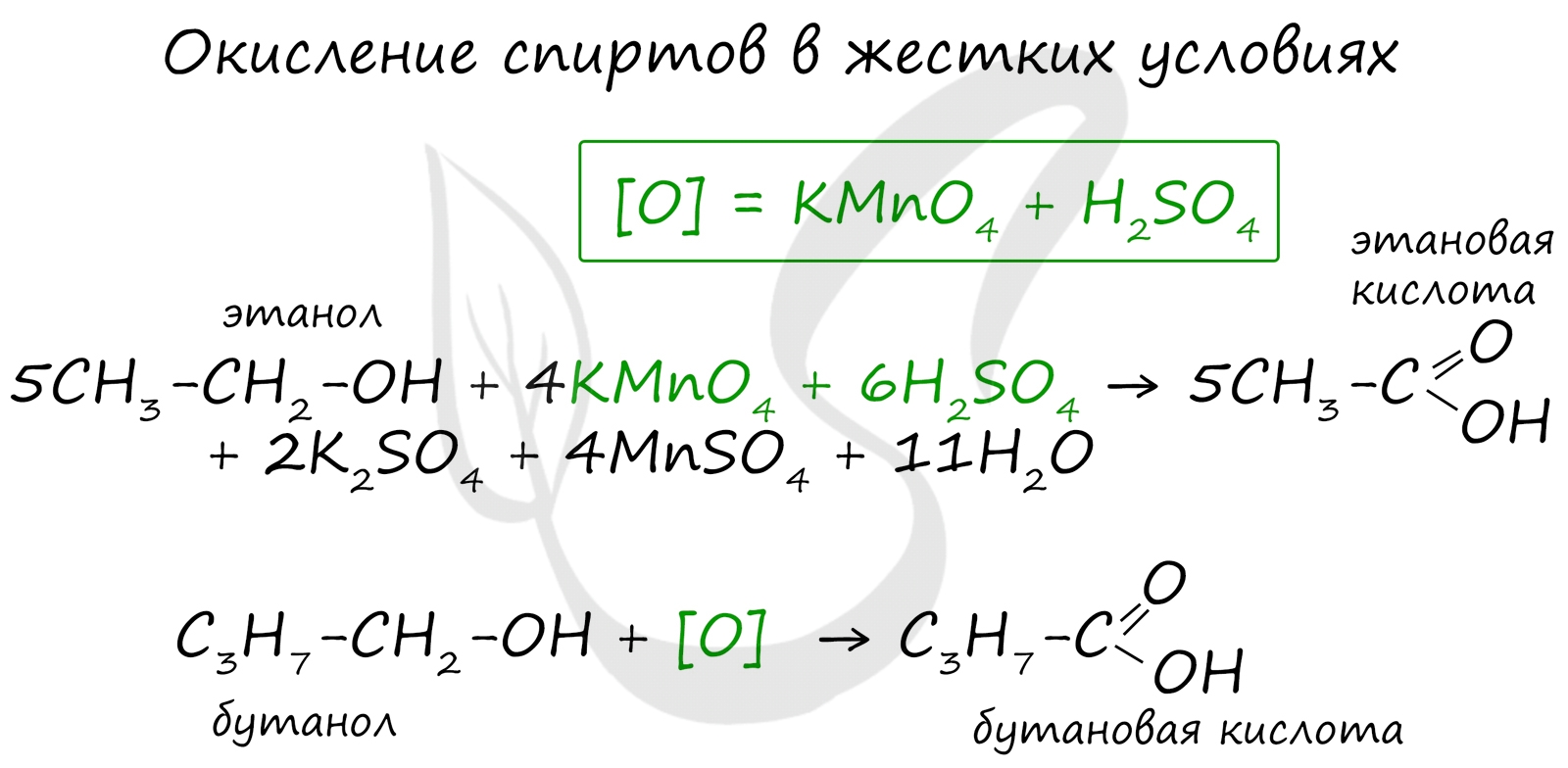
При окислении альдегиды образуют соответствующие карбоновые кислоты. Окисление можно проводить качественной реакцией на альдегиды - реакцией серебряного зеркала.

Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.

Окисление альдегидов также может быть успешно осуществлено другим реагентом - свежеосажденным гидроксидом меди II. В результате такой реакции образуется осадок кирпично-красного цвета оксида меди I.
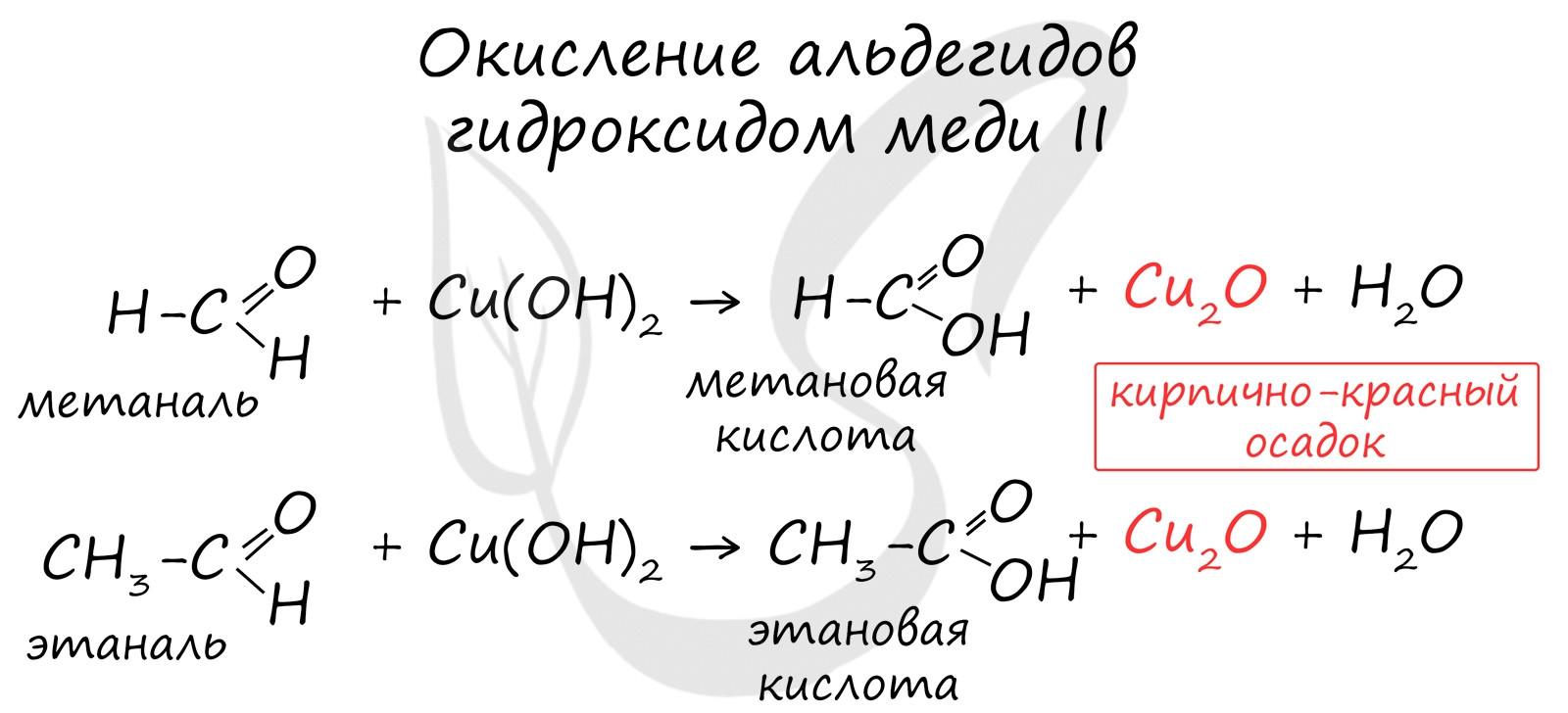
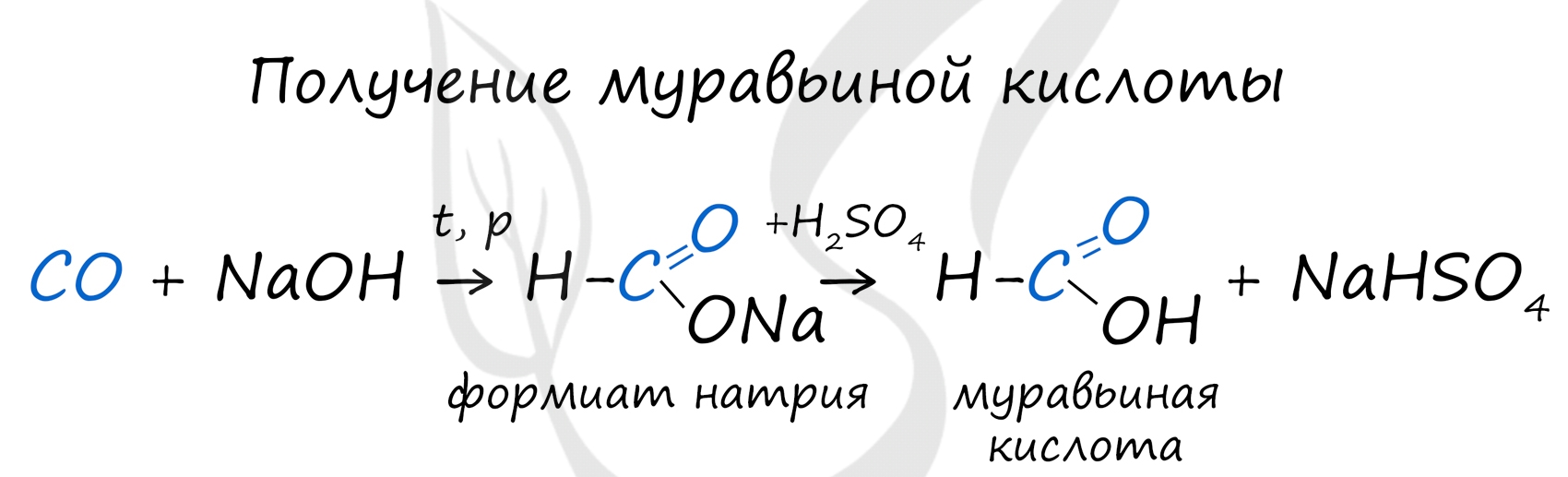
Существует специфический способ получения муравьиной кислоты, который заключается в реакции твердого гидроксида щелочного металла с угарным газом под давлением и температуре 200°С - образуется формиат (соль муравьиной кислоты).
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
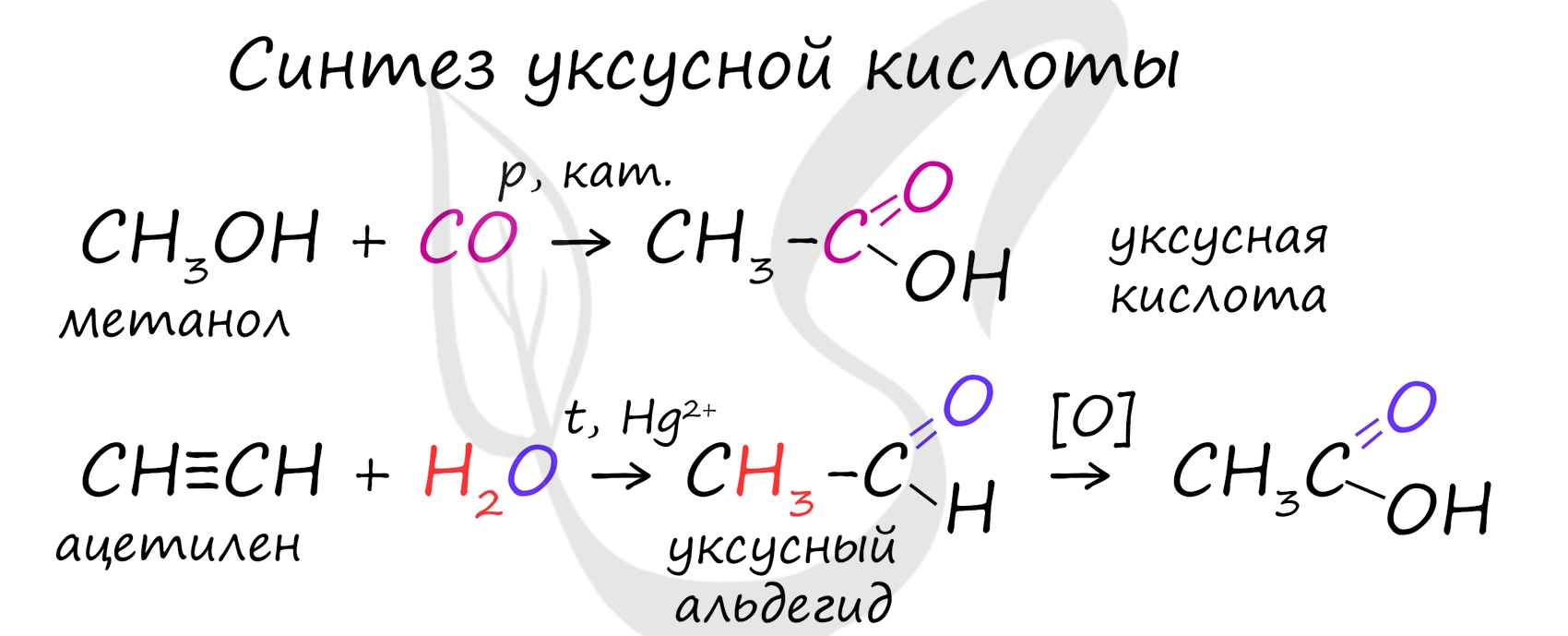
Химические свойства карбоновых кислот
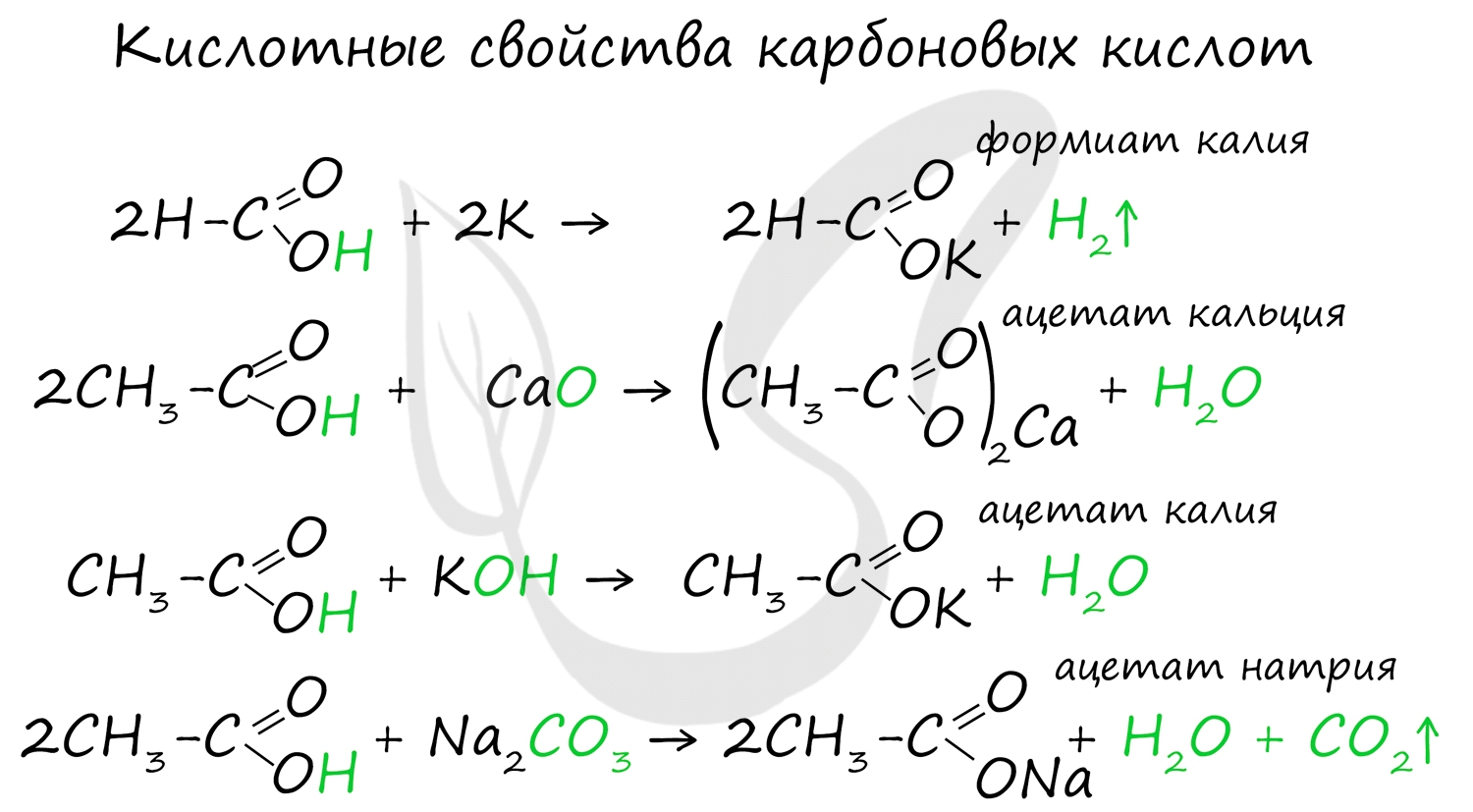
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
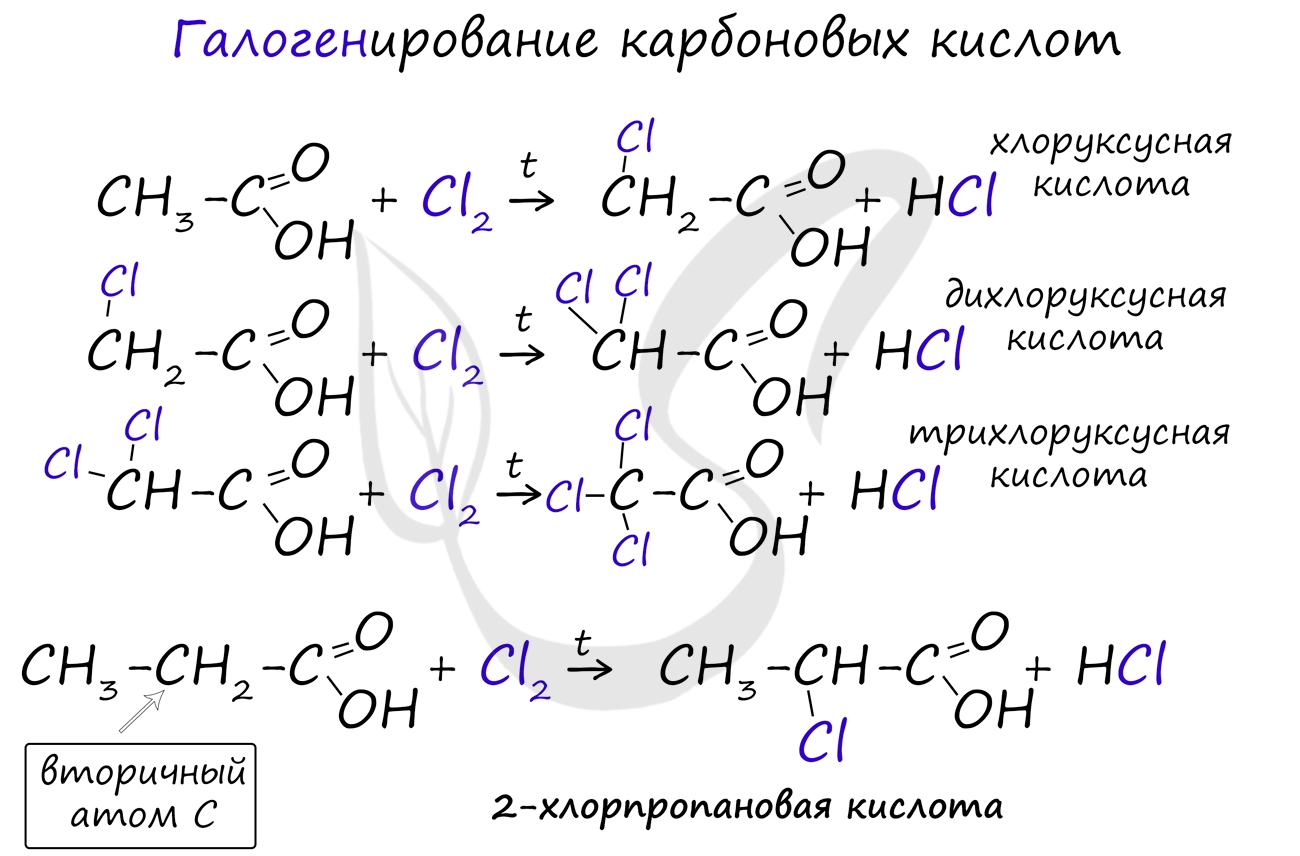
Галогенирование происходит по типу замещения в радикале, который соединен с карбоксильной группой. Напомню, что наиболее легко замещается водород у третичного, чуть сложнее - у вторичного, и значительно сложнее - у первичного атома углерода.
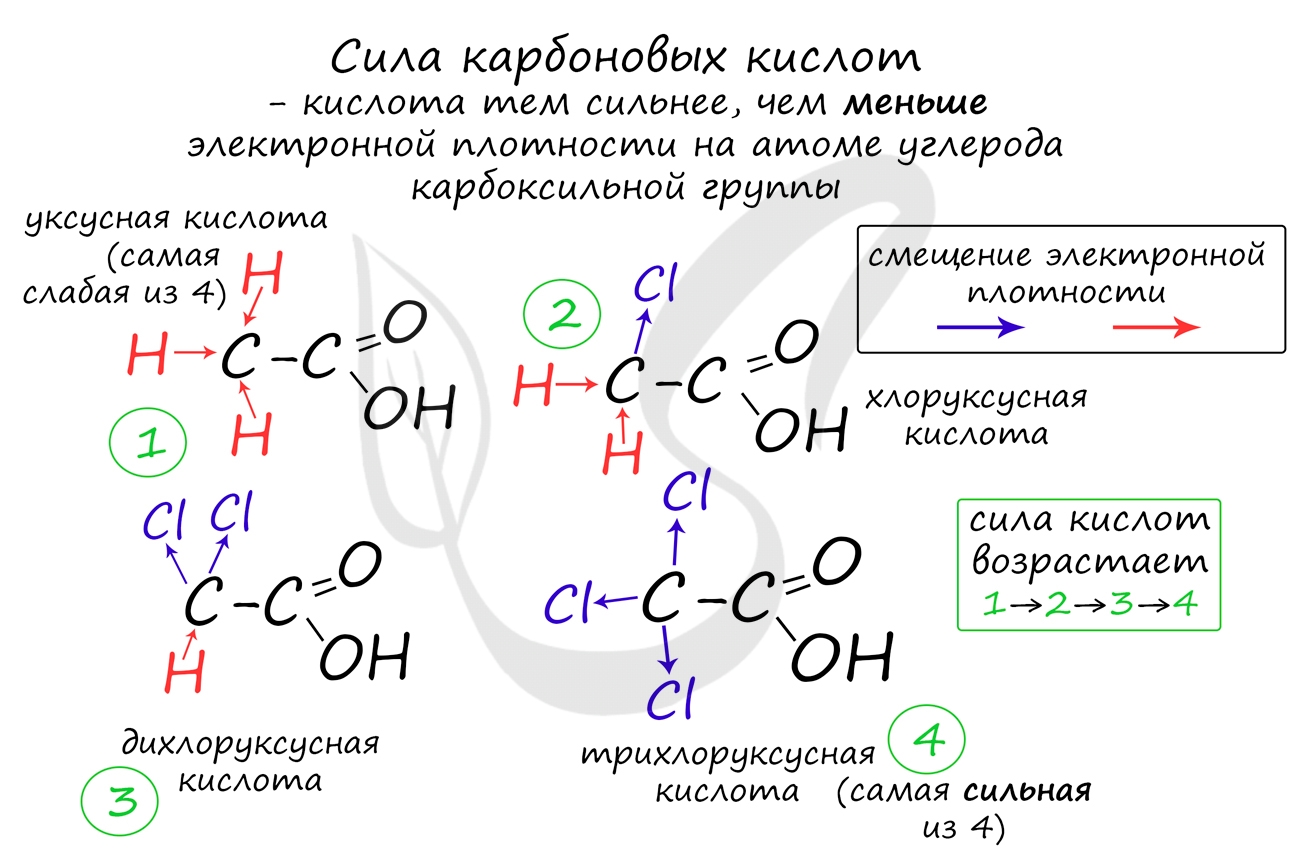
Сила карбоновых кислот тем выше, чем меньше электронной плотности сосредоточено на атоме углерода в карбоксильной группе. Поэтому самая слабая из трех кислот - уксусная, чуть сильнее - хлоруксусная, за ней - дихлоруксусная и самая сильная - трихлоруксусная.
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
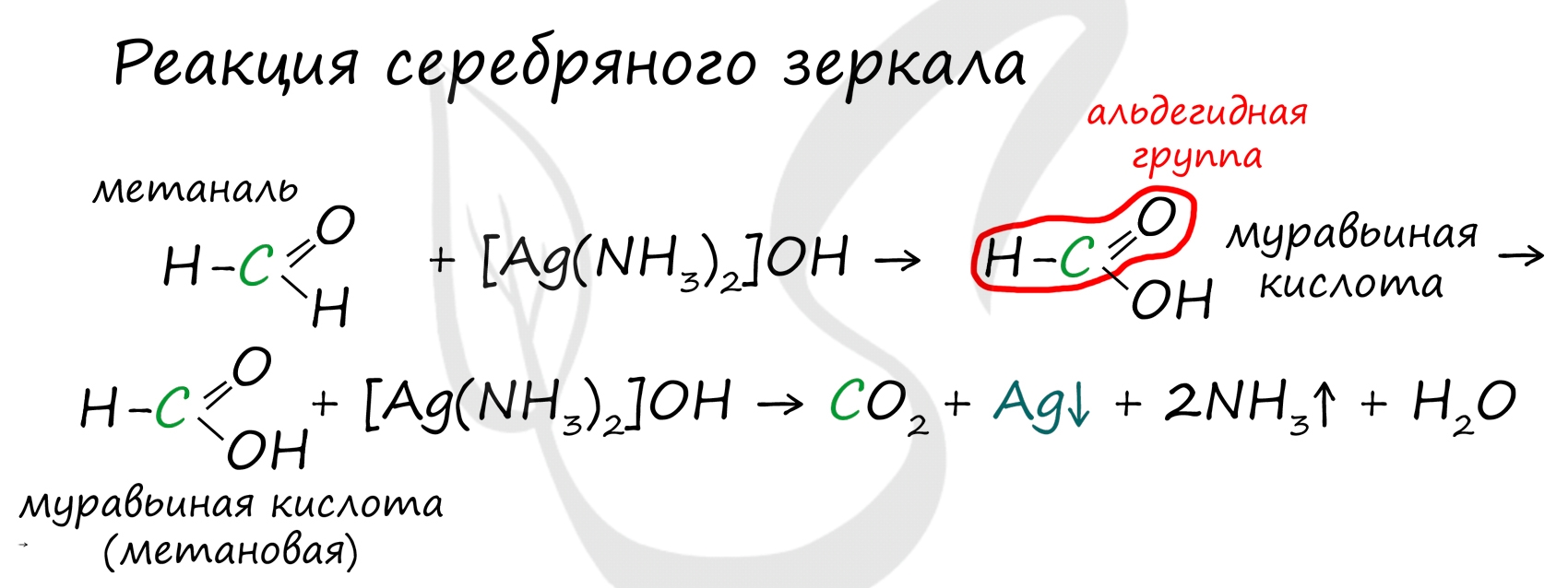
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
Сложные эфиры
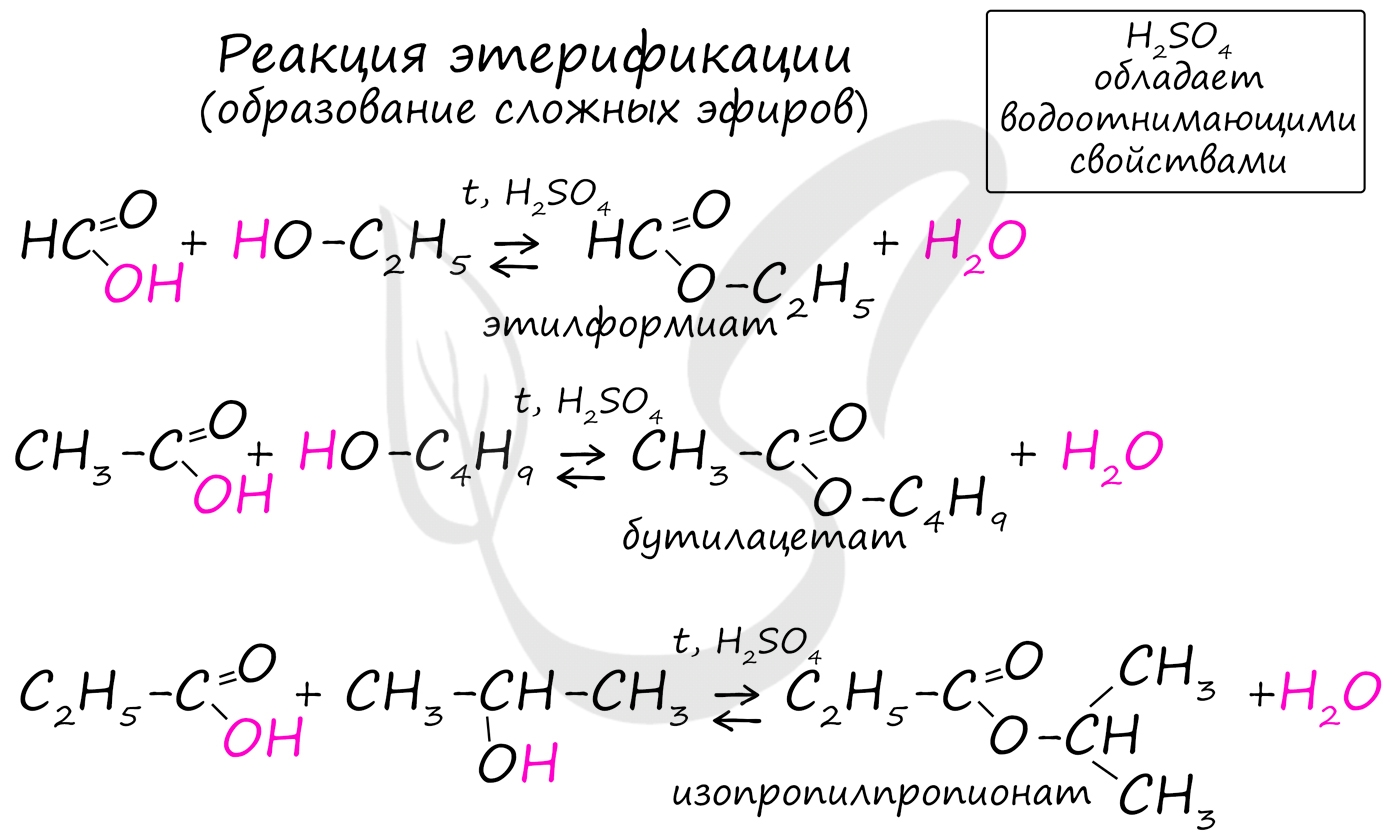
Получение сложных эфиров происходит в реакции этерификации (лат. aether - эфир), заключающейся во взаимодействии карбоновой кислоты и спирта.
Названия сложных эфиров формируются в зависимости от того, какой кислотой и каким спиртом эфир образован. Примеры:
- Метановая кислота + метанол = метиловый эфир метановой кислоты (метилформиат)
- Этановая кислота + этанол = этиловый эфир уксусной кислоты (этилацетат)
- Метановая кислота + этанол = этиловый эфир метановой кислоты (этилформиат)
- Пропановая кислота + бутанол = бутиловый эфир пропионовой кислоты (бутилпропионат)
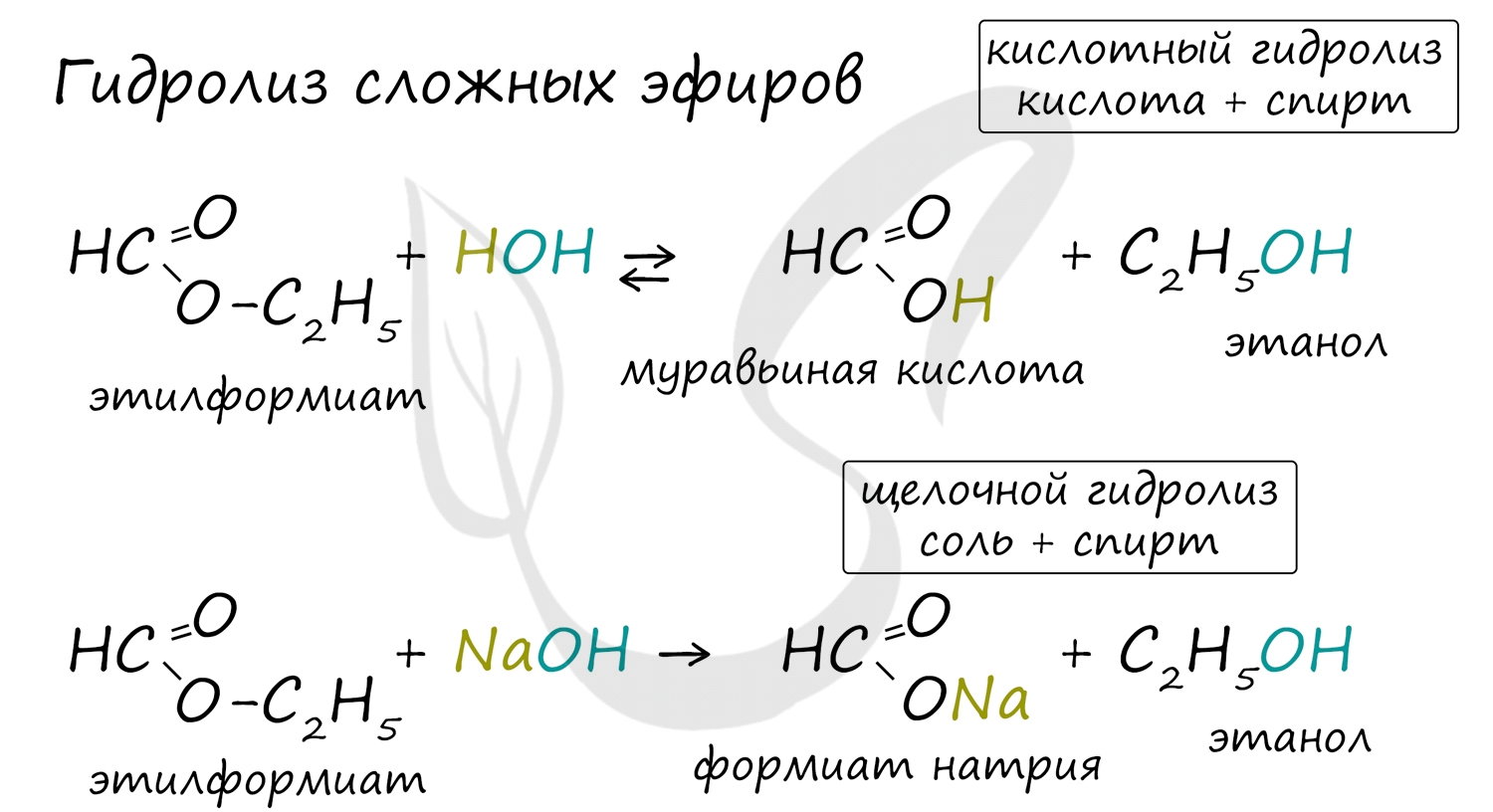
Для сложных эфиров характерной реакцией является гидролиз - их разложение. Возможен щелочной гидролиз, при котором образуется соль кислоты и спирт, и кислотный гидролиз, при котором образуются исходные спирт и кислота.
Кислотный гидролиз протекает обратимо, щелочной - необратимо. Реакция щелочного гидролиза по-другому называется реакция омыления, и напомнит о себе, когда мы дойдем до темы жиров.
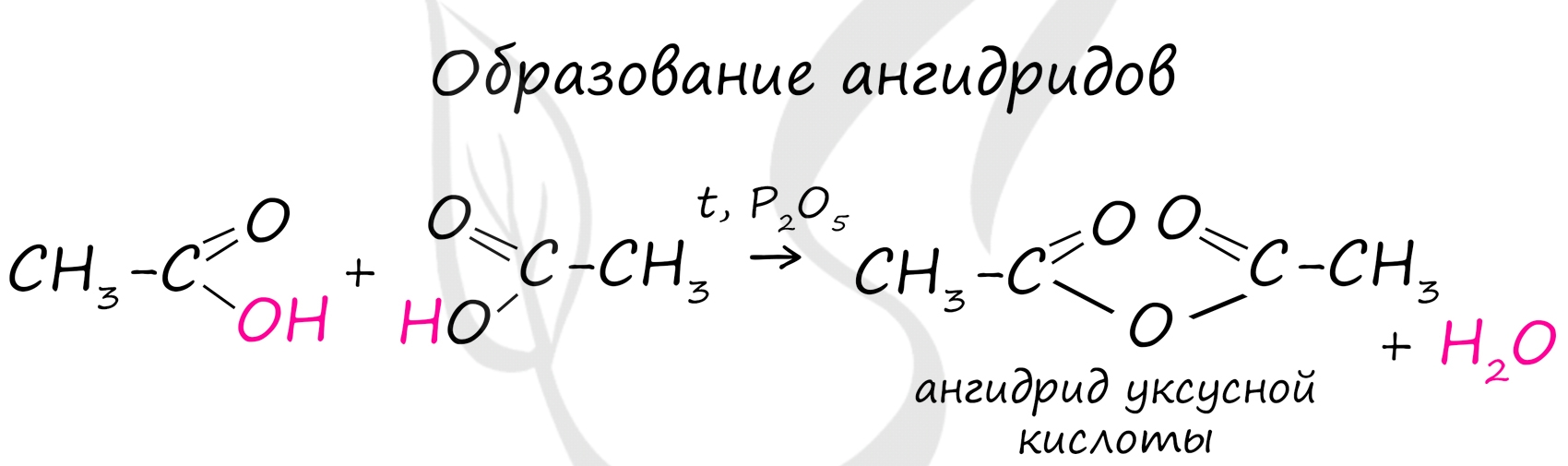
Ангидриды
Ангидриды - химические соединения, производные неорганических и органических кислот, образующиеся при их дегидратации.
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
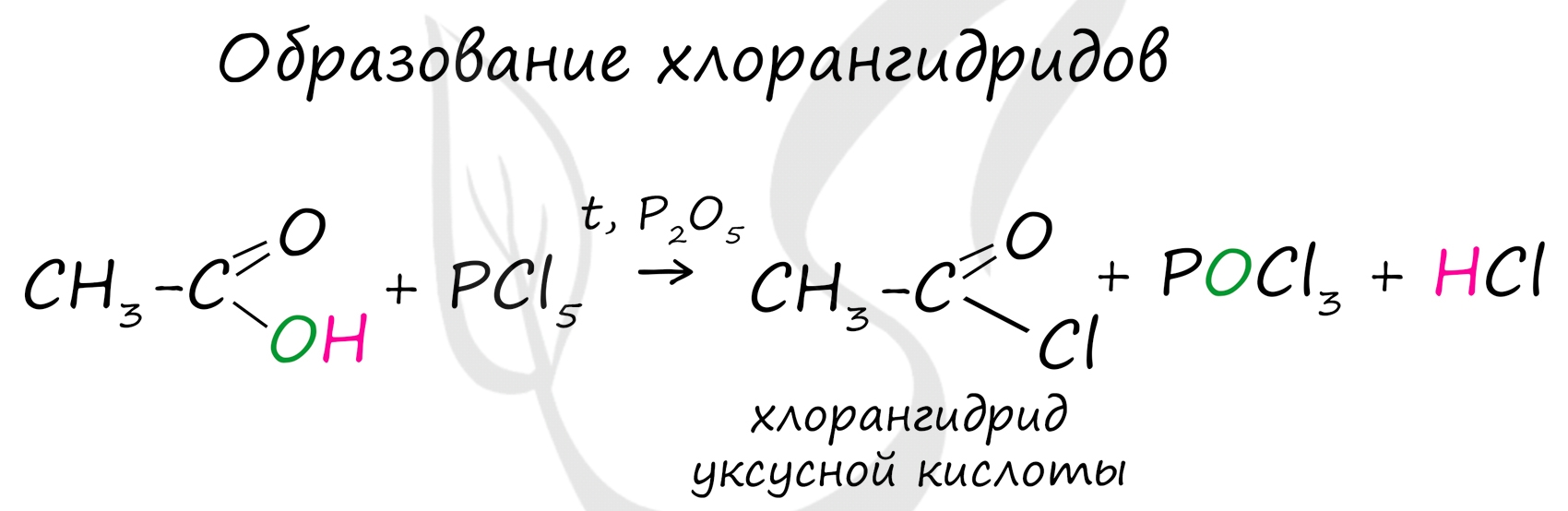
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
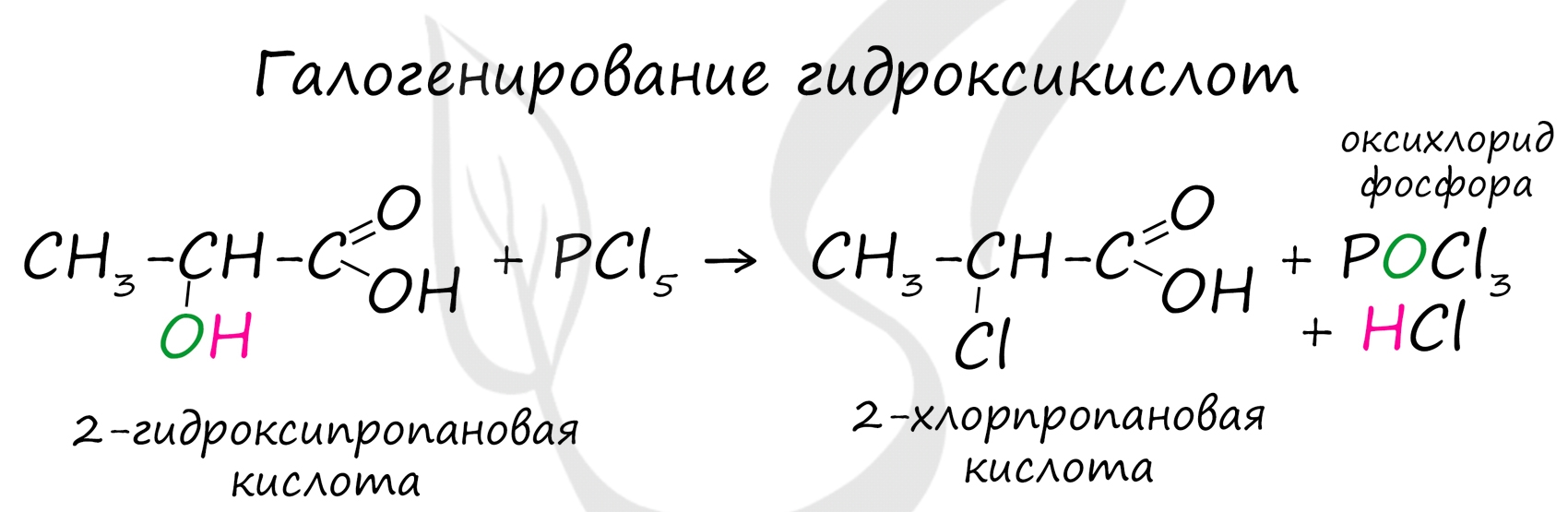
Непредельные карбоновые кислоты
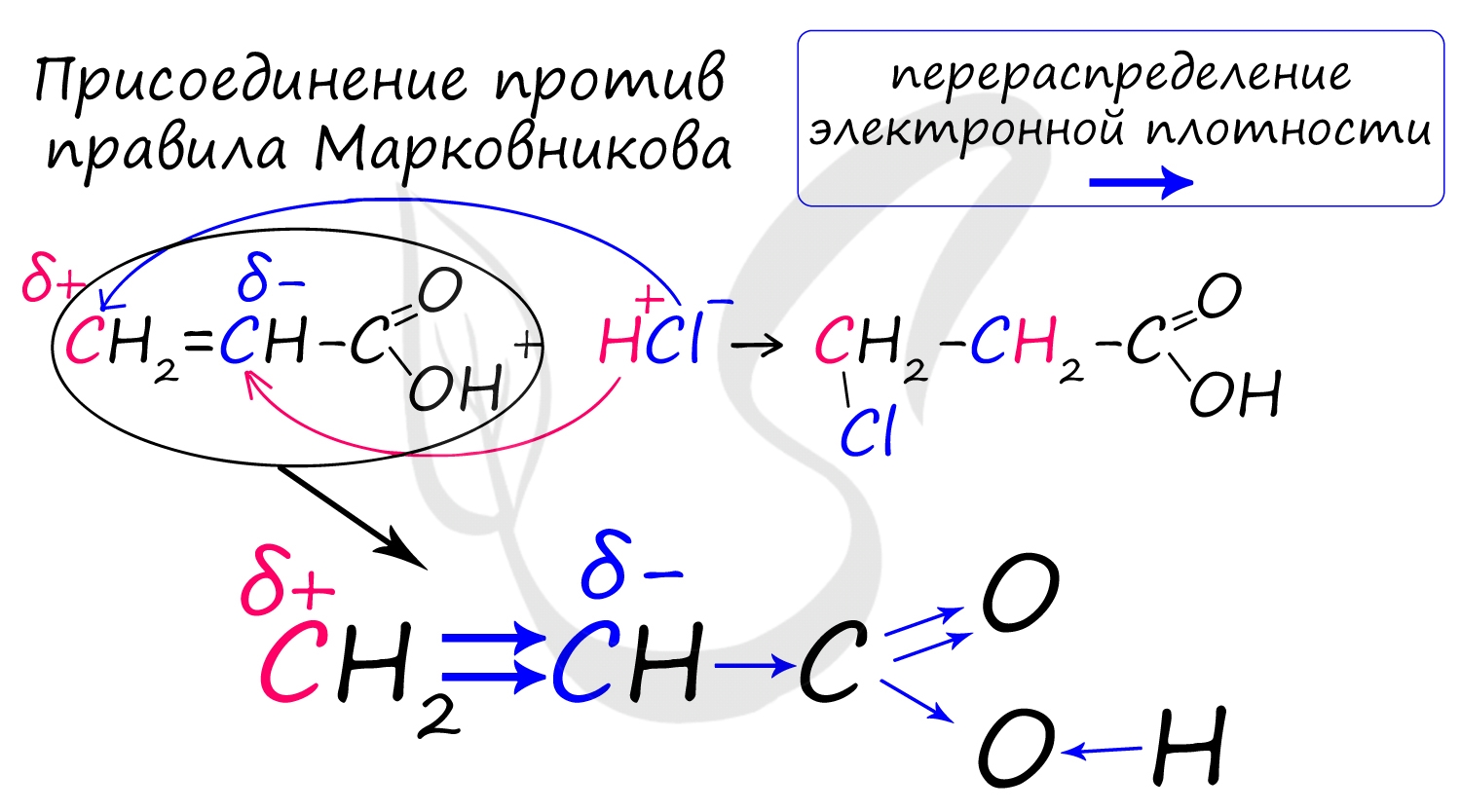
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
I- вариант
Карбоновые кислоты
Строение и номенклатура
1 . Состав карбоновых кислот отражает общая формула
1) RCOOR 2) RCOH 3) ROH 4) RCOOH
2. Функциональная группа карбоновых кислот состоит из.
1) карбонильной и аминогруппы
2) гидроксильной и аминогруппы
3) карбонильной и гидроксильной группы
4) карбонильной и нитрогруппы
3. Укажите формулу кислоты, являющейся альдегидокислотой
1) С 17 Н 31 СООН 2) HCOOH 3) СН 3 СООН 4) С 15 Н 31 СООН
4. Назовите соединение:
СН 3 – СН 2 - С(СН 3 ) 2 – СН 2 – СООН
2) 3-метилпентановая кислота
4) 3,3-диметилпентановая кислота
5.Уксусную кислоту можно получить реакцией с Cu ( OH ) 2 вещества
1) этанол 2) пропанол 3) этаналь 4) метаналь
6.Бутановая кислота образуется в результате взаимодействия
1) бутаналя с гидроксидом меди(II)
2) бутена-1 с гидроксидом меди(II)
3) бутана с серной кислотой
4) бутанола-1 с серной кислотой
Химические свойства карбоновых кислот
7.Аммиачный раствор оксида серебра является реактивом на
8. Уксусная кислота не взаимодействует с
9.Пропионовая кислота реагирует с
1) гидроксидом калия
2) бромной водой
3) уксусной кислотой
10.Из предложенного перечня выберите два вещества, с которыми взаимодействует муравьиная кислота
1) сульфат кальция
2) гидроксид бария
3) нитрат меди (II)
5) оксид углерода (II)
Верны ли следующие суждения
11.Верны ли следующие суждения о свойствах предельных карбоновых кислот
А. Все кислоты являются жидкостями при нормальных условиях.
Б. При взаимодействии со спиртами образуют сложные эфиры.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
12.Верны ли следующие суждения о свойствах пропионовой кислоты?
А. Пропионовая кислота слабее, чем соляная.
Б. Для пропионовой кислоты характерны реакции присоединения.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Установите соответствие
13. Установите соответствие между реагирующими веществами и органическим веществом – продуктом этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
ОРГАНИЧЕСКИЙ ПРОДУКТ РЕАКЦИИ
А) уксусная кислота и этанол
Б) уксусная кислота и гидроксид меди (II)
В) уксусная кислота и карбонат натрия
Г) уксусная кислота и хлор
1) хлоруксусная кислота
2) этилат натрия
3) ацетат натрия
4) ацетат меди (II)
Генетическая связь между классами неорганических соединений
14.В схеме превращений
веществом « Х » является
15. Сумма коэффициентов молекулярном уравнении реакции между оксидом кальция и уксусной кислотой равна
1) 5 2) 7 3) 6 4) 4
16. Формула карбоновой кислоты с М= 60г/моль
II вариант
Строение и номенклатура
1. К предельным одноосновным карбоновым кислотам относится вещество, формула которого
2. Функциональная группа карбоновых кислот называется
карбонильной 2) гидроксильной 3) карбоксильной 4) сложноэфирной
3. Назовите карбоновую кислоту С 3 Н 7 СООН
4. Назовите соединение СН 3 –СН(СН3)- СН 2 -СН 2 -СООН
1) 2-метилпентеновая кислота 2) 4-метилбутановая кислота
3) 2-метилпентановая кислота 4) 4-метилпентановая кислота
5. Муравьиную кислоту можно получить
1) восстановлением метаналя
2) взаимодействием этилена с водой
3) окислением метаналя
4) гидратацией ацетилена
6. Пентановая кислота образуется в результате взаимодействия
1) пентана с серной кислотой
2) пентена-1 с водой
3) пентанола-1 с гидроксидом натрия
4) пентаналя с гидроксидом меди (II) проверить
Химические свойства карбоновых кислот
7. Кислотные свойства уксусной кислоты проявляются в реакции с
1) медью 2) карбонатом натрия 3) кислородом 4) бромом
8. Ацетат натрия не получится при действии на уксусную кислоту
1) натрия 2) гидроксида натрия 3) карбоната натрия 4) хлорида натрия
9.Пропановая кислота взаимодействует с
3) карбонатом натрия
4) ацетатом натрия
5) гидроксидом бария
6) сульфатом меди(II)
10.Из предложенного перечня выберите два вещества, с которыми взаимодействует муравьиная кислота
1) оксид углерода(II)
2) аммиачный раствор оксида серебра
3) карбонат кальция
4) сульфат кальция
5) нитрат меди(II)
Верны ли следующие суждения
11.Верны ли следующие утверждения о свойствах предельных карбоновых кислот?
А. Карбоновые кислоты образуются при окислении первичных спиртов и альдегидов.
Б. Для карбоновых кислот характерна реакция гидролиза.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
12.Верны ли следующие суждения о свойствах муравьиной кислоты?
А. Вступает в реакцию с аммиачным раствором оксида серебра.
Б. Является одноосновной кислотой.
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
Установите соответствие
13.Установите соответствие между реагирующими веществами и органическим веществом – продуктом этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
ПРОДУКТ РЕАКЦИИ
А) уксусная кислота и натрий
Б) уксусная кислота и аммиак (р-р)
В) уксусная кислота и метиловый спирт
Г) уксусная кислота и хлорид фосфора ( V )
2) ацетат аммония
3) ацетат натрия
5) ацетилхлорид (хлорангидрид уксусной кисоты)
6) аминоуксусная кислота
Генетическая связь между классами неорганических соединений
14.В схеме превращений
С2 H 2 Х CH3COOH
веществом « Х » является
15. Сумма коэффициентов молекулярном уравнении реакции между оксидом магния и уксусной кислотой равна
16. Формула карбоновой кислоты с М= 74 г/моль



- Все материалы
- Статьи
- Научные работы
- Видеоуроки
- Презентации
- Конспекты
- Тесты
- Рабочие программы
- Другие методич. материалы
Тест предназначен для закрепления знаний на уроке по теме "Карбоновые кислоты" для 10 класса и 1 курса групп СПО. Тест составлен в двух вариантах. Разделы теста: Строение и номенклатура. Получение. Химические свойства карбоновых кислот. Генетическая связь между классами неорганических соединений.
- Бурбело Ирина АлександровнаНаписать 22032 28.04.2019
Номер материала: ДБ-570808
- Химия
- 10 класс
- Тесты
-
23.04.2019 120
-
23.04.2019 226
-
23.04.2019 1292
-
13.04.2019 173
-
01.04.2019 324
-
25.03.2019 116
-
09.03.2019 847
-
06.03.2019 165
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.

Главная Помощь Войти Настройки
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg + | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH - | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | - | - | Н | Н | Н | |
| F - | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | - | Н | Р | Р |
| Cl - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | - | - | - | Н | - | - | Н | - | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | - | Н | ? | Н | Н | ? | М | М | - | Н | ? | ? |
| HSO3 - | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | - | Н | Р | Р |
| HSO4 - | Р | Р | Р | Р | Р | Р | Р | Р | - | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р |
| NO2 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | - | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO - | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р | Р | - | Р | Р | Р | Р | Р | Р | Р | - | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые (
Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2
Скопируйте эту ссылку, чтобы разместить результат запроса " " на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса " " содержит ошибку, нажмите на кнопку "Отправить". Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки - помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация - такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений.
Здесь, возможно, указаны не все изомеры данного вещества. Более полный поиск изомеров следует проводить по формуле. Например, чтобы получить изомеры вещества с формулой С6H10O2 , следует сделать запрос так: Изомеры - это соединения с одинаковым количественным составом (то есть одинаковым числом атомов каждого элемента), но разным строением. Корректная работа сайта обеспечена на всех браузерах, кроме Internet Explorer. Если вы пользуетесь Internet Explorer, смените браузер. Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды). 2. Вещество, подвергающееся гидролизу, - это 3. В порядке усиления кислотных свойств расположены кислоты 1) стеариновая - уксусная - трихлоруксусная 2) уксусная - стеариновая - трихлоруксусная 3) трихлоруксусная - уксусная - стеариновая 4) стеариновая - трихлоруксусная - уксусная 4. Жидкие растительные масла не вступают в реакцию с 2) раствором перманганата калия 4) раствором гидроксида натрия 5. При кислотном гидролизе этилацетата образуются 1) этанол и муравьиная кислота 2) этанол и уксусная кислота 3) метанол и муравьиная кислота 4) метанол и уксусная кислота 6.Формиат калия не получится при действии на муравьиную кислоту 1) гидроксида калия 2) карбоната калия 3) сульфата калия 7.Твёрдые жиры можно получить из жидких масел 2) угарного газа с кислородом 8.С помощью гидроксида меди(II) можно различить 1) толуол и пропанол 2) ацетон и винилбензол 3) пропанол и пропаналь 4) муравьиный альдегид и пропионовый альдегид 9.Фруктоза образуется в результате гидролиза 10. Среди утверждений: А. В карбонильной группе альдегидов электронная плотность смещена к атому кислорода. Б. Для предельных альдегидов характерна геометрическая (цис-транс-) изомерия. 1) верно только А 2) верно только Б 3) верны оба утверждения 4) неверны оба утверждения 11. Ацетальдегид не реагирует с 1) аммиачным раствором оксида серебра 2) гидроксидом меди(II) 4) гидроксидом натрия 12. В порядке усиления кислотных свойств расположены кислоты 1) уксусная – трихлоруксусная- муравьиная 2) уксусная - муравьиная- трихлоруксусная 3) трихлоруксусная - уксусная - муравьиная 4) трихлоруксусная -муравьиная- уксусная 13. Гидратацией алкина может быть получен 3) пропионовый альдегид 4) масляный альдегид 14. Уксусная кислота не реагирует с 3) хлоридом натрия 4) карбонатом калия 15.Продуктом восстановления пропаналя является 2) пропановая кислота 16. В цепи превращений C2H5OH ? X ? CH3COOH веществом Х является 17. Спирт может быть получен при взаимодействии альдегида 1) с гидроксидом меди(II) 3) с водородом на катализаторе 4) с хлороводородом 18.В цепи превращений CH3COOH ? X ? H2N-CH2-COOH веществом Х является 1) уксусный альдегид 4) хлоруксусная кислота 19. Для формальдегида характерны реакции 20. В цепи превращений CH3COOH + Na2CO3 ?X1 Х1+ конц. H2SO4 ?X2 веществами Х1 и Х2 являются соответственно 2) CH3COONa и CH3COOH 3) CH3COONa и C2H5OH 4) CH3CH=O и C2H5OH 21.Формальдегид не реагирует с 1) C6H5 - OH 2) Cu(OH)2 3) H2 4) NaOH 22. С гидрокарбонатом натрия реагирует каждое из веществ 1) HCOOH и CH3COOH 2) CH3COOH и C2H5OH 3) C2H5OH и C6H5OH 4) C6H5OH и CH2OH - CH2OH 23. Продуктом окисления пропаналя является 2) пропановая кислота 24. Муравьиная кислота реагирует с 1) хлоридом натрия 2) аммиачным раствором оксида серебра 25. Свойства альдегида не проявляет 26. Ацетат натрия не получится при действии на уксусную кислоту 2) гидроксида натрия 3) хлорида натрия 4) карбоната натрия 27. Вступают с водородом в реакцию присоединения 1) пропанол и бензол 2) бензол и ацетальдегид 3) ацетальдегид и пропан 4) пропан и метиламин 28. Для муравьиной кислоты не характерна реакция 2) «серебряного зеркала» 29. С аммиачным раствором оксида серебра реагирует 2) уксусная кислота 30. Уксусная кислота реагирует с 4) хлоридом натрия Ответы: 1-4, 2-4, 3-1, 4-3, 5-2, 6-3, 7-4, 8-3, 9-3, 10-1, 11-1, 12-2, 13-2, 14-3, 15-1, 16-3, 17-3, 18-4, 19-2, 20-2, 21-4, 22-1, 23-2, 24-2, 25-3, 26-3, 27-2, 28-2, 29-1, 30-1. Читайте также:
|


