Что объединяет золото серебро медь олово
Опубликовано: 24.07.2024
Химические элементы, образующие в свободном состоянии простые вещества с металлической связью. Из 107 известных химических элементов (см. Периодическая система химических элементов) 85-металлы и только 22-неметаллы.
Такие металлы, как золото, серебро и медь, известны человеку с доисторических времен. В древние и средние века считали, что существует только 7 металлов (золото, серебро, медь, олово, свинец, железо и ртуть). М. В. Ломоносов определял металл как "светлое тело, которое ковать можно" и относил к металлам золото, серебро, медь, олово, железо и свинец. Л. Лавуазье в "Начальном курсе химии" (1789) упоминал уже 17 металлов. В начале XIX в. последовало открытие платиновых металлов, затем щелочных, щелочноземельных и ряда других.
Триумфом периодического закона было открытие металлов, предсказанных на его основе Д. И. Менделеевым,- галлия, скандия и германия. В середине XX в. с помощью ядерных реакций были получены трансурановые элементы - не существующие в природе радиоактивные металлы.
Современная металлургия получает свыше 75 металлов и на их основе более 5000 сплавов.
В основе структуры металлов лежит кристаллическая решетка из положительных ионов, погруженная в плотный газ подвижных электронов. Эти электроны компенсируют силы электрического отталкивания между положительными ионами и тем самым связывают их в твердые тела.
Такой тип химической связи называют металлической связью. Она обусловила важнейшие физические свойства металлов: пластичность, электропроводность, теплопроводность, металлический блеск.
Пластичность - это способность металлов изменять форму при ударе, прокатываться в тонкие листы и вытягиваться в проволоку. При этом происходит смещение атомов и ионов кристаллической решетки, однако связи между ними не разрываются, так как соответственно перемещаются и электроны, образующие связь. Пластичность металлов уменьшается в ряду Au, Ag, Си, Sn, Pb, Zn, Fe. Золото, например, можно прокатывать в листы толщиной до 0,003 мм, которые используют для золочения.
Высокая электропроводность металлов объясняется присутствием свободных электронов, которые под влиянием даже небольшой разности потенциалов перемещаются от отрицательного полюса к положительному. С повышением температуры колебания ионов и атомов металлов усиливаются, что затрудняет движение электронов и тем самым приводит к уменьшению электропроводности. При низких же температурах колебательное движение ионов и атомов, наоборот, сильно уменьшается, и электропроводность возрастает. Вблизи абсолютного нуля электрическое сопротивление у металлов практически отсутствует. Лучший проводник электричества - серебро, за ним идут медь, золото, алюминий, железо. Также изменяется и теплопроводность металлов, которая вызвана как высокой подвижностью свободных электронов, так и колебательным движением ионов, благодаря чему происходит быстрое выравнивание температуры в массе металла. Металлический блеск тоже связан с наличием свободных электронов.
Из других физических свойств металлов наибольший практический интерес представляют плотность, температура плавления и твердость. Самый легкий из металлов - литий (плотность 0,53 г/см 3 ), самый тяжелый - осмий (22,6 г/см 3 ). Металлы с плотностью меньше 5 г/см 3 называются легкими, остальные - тяжелыми. Температуры плавления металлов различаются очень сильно: цезий и галлий можно расплавить теплом ладоней, а температура плавления вольфрама + 3410°С. При обычных условиях единственный жидкий металл - ртуть. В парообразном состоянии все металлы одноатомны, их кристаллическая решетка разрушается.
Металлы различаются по твердости. Самый твердый из них - хром - режет стекло, а самые мягкие - калий, рубидий и цезий -легко режутся ножом. Прочность, температура плавления и твердость зависят от прочности металлической связи. Она особенно велика у тяжелых металлов.
В технике сплавы на основе железа, т.е. чугун, сталь, а также само железо называются черными металлами, все остальные металлы называются цветными. Существуют и другие классификации металлов (см. Периодическая система химических элементов).

Металлы - химические элементы, способные отдавать внешние (валентные) электроны. В древности и в средние века было известно 7 металлов: золото, серебро, медь, олово, свинец, железо, ртуть. Многие века алхимики тщетно искали способы превращения металлов в золото. Железо служило для изготовления оружия и орудий труда. Свое ведущее место железо сохраняет и в наши дни. Особенно широко оно используется в металлургии. Важную роль в современной технике играют алюминий, медь и другие металлы
Химические свойства металлов определяются слабой связью валентных электронов с ядром атома. Атомы сравнительно легко отдают их, превращаясь при этом в положительно заряженные ионы. Поэтому металлы являются хорошими восстановителями. В этом их главное и наиболее общее химическое свойство.
Очевидно, как восстановители металлы должны вступать в реакции с различными окислителями, среди которых могут быть простые вещества (неметаллы), кислоты, соли менее активных металлов и некоторые другие вещества. Соединения металлов с кислородом называются оксидами, с галогенами - галогенидами, с серой - сульфидами, с азотом - нитридами, с фосфором - фосфидами, с углеродом -карбидами, с кремнием - силицидами, с бором - боридами, с водородом - гидридами и т. д. Многие из этих соединений нашли важное применение в технике.
При взаимодействии металлов с кислотами окислителем является ион водорода Н + , который принимает электрон от атома металла:
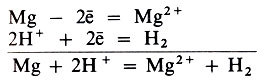
Все металлы, стоящие в ряду стандартных электродных потенциалов (ряду напряжений) левее водорода, вытесняют (восстанавливают) водород из разбавленных кислот типа НСl или H2SO4, а металлы, стоящие правее водорода, его не вытесняют.
Взаимодействие металлов с водными растворами солей менее активных металлов можно иллюстрировать примером:
В этом случае происходит отрыв электронов от атомов более активного металла - цинка и присоединение их ионами менее активного Сu 2+ . Руководствуясь рядом стандартных электродных потенциалов, можно сказать, что каждый металл вытесняет (восстанавливает) из растворов их солей все следующие за ним металлы.
Активные металлы (щелочные и щелочноземельные) взаимодействуют и с водой, которая в этом случае выступает в роли окислителя.
Металлы, гидроксиды которых амфотерны (см. Амфотерность), как правило, взаимодействуют с растворами и кислот, и щелочей.
Металлы могут образовывать химические соединения между собой. Такие соединения обычно образуют типичные металлы с металлами, обладающими слабыми металлическими свойствами, например определенные соединения натрия со свинцом:
Соединения одних металлов с другими носят общее название интерметаллидов, интерметаллических соединений, или металлидов.
Рассмотренные свойства металлов, связанные с отдачей электронов в химических реакциях, называют металлическими. В различной степени ими обладают все химические элементы. О металлических свойствах судят, сопоставляя электроотрицательности элементов. Эта величина, выраженная в условных единицах, характеризует способность атома в молекуле притягивать электроны. Относительные значения электроотрицательностей элементов приведены в таблице на с. 342. Чем меньше электроотрицательность, тем сильнее выражены металлические свойства элемента.
Медь, серебро и золото – эти металлы были в числе первых, освоенных человеком. Из них чеканили монеты, изготовляли предметы домашнего обихода, орудия труда и украшения.
Со временем серебро и особенно золото стали универсальным мерилом материальных ценностей. Получение золота из других металлов составляло предмет алхимии – ярчайшей страницы в истории человеческой мысли, давшей начало современной химии. С тех пор жизнь людей почти до неузнаваемости изменилась, а золото по-прежнему является символом богатства и эталоном ценности…
Медь

Латинское наименование меди – Cuprum – происходит от названия острова Кипр, где уже в III в до н.э. существовали медные рудники. Русское «медь», вероятно, восходит к слову «смида», обозначавшему металл у древних германцев.
Хоть медь иногда встречается в природе в виде самородков (самый большой из найденных весил 420 т), основная её часть входит в состав сульфидных руд, например халькопирита CuFeS2. Реже встречается минерал малахит – зеленый основной карбонат меди (CuOH)2CO3.
В первых металлургических процессах использовались не сульфидные руды, а именно малахит, не требующий предварительного обжига. Восстановительную плавку проводили в глиняных сосудах, заполненных рудой и углем и помещенных в небольшую яму. Оксид углерода (II), образуется при неполном сгорании угля, восстанавливая малахитовую руду:
Развивающаяся при этом температура (1100 – 1200 о С) позволяет получить расплавленную медь (tпл = 1083 о С).
Медь весьма мягкий металл, поэтому начиная с III тысячелетия до н.э. на смену медным изделиям стали приходить бронзовые – более твёрдые и прочные. Скорее всего, бронзу (сплав меди с оловом) впервые получили случайно, при обработке руды, содержащей оба металла. На протяжении двух тысяч лет (до начала I тысячелетия до н.э.) бронза являлась основным материалом для производства орудий труда. Археологи называют эту эпоху бронзовым веком.

Чистая медь очень хорошо проводит электрический ток, уступая в этом лишь серебру, поэтому из нее делают провода. Сплав меди с никелем – константан (60% Cu,40% Ni), напротив, отличается высоким сопротивлением – он служит основой реостатов. Бронзы (90% Cu, 10% Sn) и латуни (20 – 80% Cu, остальное Zn) твёрже меди, стойки к окислению, обладают малым коэффициентом трения. Они используются в химическом машиностроении и для изготовления подшипников, шестерен, редукторов. Нейзильбер — сплав состава 50% Cu, 25% Zn, 25% Ni – применяется в производстве медицинского оборудования и в ювелирном деле. Медно-никелевый сплав мельхиор (80% Cu, 20% Ni) идет на изготовление медицинских инструментов, монет, посуды.
Медь применяют в гальванопластике – получении точных металлических копий различных предметов путем электролитического осаждения металла на поверхности гипсовой формы.
Ежегодно в мире выплавляют приблизительно 10 млн тонн меди, и потребность в этом металле постоянно возрастает.
В отличие от своих соседей по подгруппе – серебра и золота,- медь непосредственно реагирует с кислородом. При нагревании на воздухе изделия чернеют, покрываясь слоем оксида меди (II) CuO. А при температуре свыше 1000 о С образуется другой оксид – Cu2O.
Находясь долгое время на воздухе, медь покрывается плёнкой малахита, образующегося по реакции 2Cu + O2 + H2O + CO2 = (CuOH)2CO3. Именно этому веществу обязаны своим цветом бронзовые памятники и старые крыши городов Западной Европы.
В ряду напряжений медь стоит правее водорода, поэтому реагирует только с кислотами-окислителями: азотной, концентрированной серной. Исключение составляет йодоводородная кислота, которая вступает в реакцию с медью с выделением водорода и образованием очень устойчивого комплекса меди (I) H[CuI2].
Пожалуй, самое известное соединение меди – медный купорос, или пятиводный сульфат меди (II), CuSO4∙5H2O. В древности это вещество получали при кристаллизации растворов, образующихся в медных рудниках во время дождя. Медный купорос применяли для чернения кожи, в медицине, производстве окрашенных стекол. В наше время медный купорос используется в сельском хозяйстве для борьбы с вредителями растений, вытеснив значительно более ядовитую соль 3Cu(AsO2)2∙Cu(CH3COO)2 – швейнфуртскую зелень.
Медь играет важную роль в процессах жизнедеятельности организмов – она входит в состав некоторых ферментов, участвующих в реакциях окисления органических соединений. Медьсодержащий фермент цитохромоксидаза катализирует процессы тканевого дыхания. Белки, в состав которых входит медь, оказывают влияние на углеводный обмен, синтез жиров, образование витаминов Р и В. Ежедневная потребность меди для человека составляет около 2 -3 мг. Особенно богаты этим элементом молоко и дрожжи. Однако в больших количествах соединения меди вредны: приём внутрь 2 г медного купороса может привести к смерти.
Серебро

Латинское название серебра – Argentum – связано с цветом этого металла; оно восходит к греческому «аргос» — «белый», «блестящий». Русское слово «серебро», как считают учёные, происходит от слова «серп» (серп луны). Блеск серебра напоминает таинственное лунное сияние и алхимикам, использовавшим в качестве символа элемента знак луны.
Древнейшие серебряные изделия, обнаруженные в Передней Азии, датируются V тысячелетием до н.э. Они изготовлены из самородного серебра. Часто такие самородки окрашены в светло-желтый цвет, так как представляют собой не чистое серебро, а сплав с золотом (греки называли его «электрон»). Находки серебряных самородков чрезвычайно редки, поэтому неудивительно, что вплоть до конца I тысячелетия до н.э. серебро стоило дороже остальных металлов, даже золота. Ситуация изменилась лишь после того, как примерно в VI в. до н.э. древние умельцы освоили процесс выделения серебра из свинцовых руд.
Некоторые свинцовые сульфидные руды, например галенит PbS, содержат значительные примеси сульфида серебра Ag2S. При обжиге такой руды на воздухе PbS переходит в оксид Pb3O4, а серебро выделяется в свободном виде:
В наши дни основную массу серебра также получают при переработке свинцово-цинковых и медных руд. Часто такая руда содержит всего 0,15 – 0,25% Ag. Выплавленный из свинцово-цинковой руды жидкий металл разделяется на два слоя: в нижнем содержится свинец, а в верхнем – цинк с примесью серебра. При нагревании этого слоя летучий цинк отгоняется в виде паров, а серебро остается.
Серебро – блестящий, серебристо-белый металл (tпл = 962 о С), ковкий и пластичный, легко поддающийся обработке, лучший среди металлов проводник тепла и электричества. В старину из него изготовляли монеты, вазы, кубки, ювелирные изделия, тончайшими серебряными пластинами украшали ларцы и одеяния. На Руси из серебра делали церковные сосуды, оклады икон. В настоящее время применение серебра не ограничивается ювелирным делом – оно идет на производство зеркал, электрических контактов, аккумуляторов, используется в стоматологии.

Серебро не окисляется кислородом, однако, по словам Плиния Старшего, «тускнеет от лечебных вод и от солёных ветров», покрываясь чёрным слоем сульфида серебра:
В ряду напряжений серебро стоит правее водорода, поэтому оно взаимодействует лишь с кислотами-окислителями, легче всего – с азотной кислотой:
Нитрат серебра (ляпис) прекрасно растворим в воде и является исходным веществом для получения других соединений серебра. При 209 о С он плавится, а при нагревании до 300 о С разлагается, образуя серебро: 2AgNO3 = 2Ag + 2NO2↑ + O2↑. Ляпис оказывает на кожу прижигающее и вяжущее действие, его используют в медицине в виде ляписных карандашей.
Гидроксид серебра AgOH является сильным основанием, однако, он настолько неустойчив, что при действии на раствор AgNO3 щёлочи выпадает не AgOH, а бурый осадок оксида Ag2O. Бесцветный раствор, образующийся при взаимодействии Ag2O с раствором аммиака: Ag2O + 2NH3 + H2O = 2[Ag(NH3)2]OH, уже в XVII в. использовали для серебрения зеркал.
В 1727 г. немецкий учёный И.Г.Шульце обнаружил, что некоторые соли серебра, например хлорид AgCl, на свету разлагаются с образованием металла. Еще легче этому подвержены AgI и AgBr – они входили в состав эмульсии чёрно-белой фотопленки.
Замечено, что болезнетворные бактерии в воде погибают уже при содержании в ней серебра 10 -9 г/л – такая концентрация ионов Ag + создаётся при внесении в воду серебряных предметов.
Золото

Еще в глубокой древности золотистый цвет металла ассоциировался в сознании людей с цветом солнца. Так, по одной из версий, русское название металла происходит от слова «солнце». Латинское название элемента (Aurum) в переводе означает «жёлтый».
Золото, не изменяющееся при хранении на воздухе, не поддающееся ржавлению, являлось символом вечности. Алхимики называли его царем металлов, совершеннейшим из всех веществ. Превращение неблагородным металлов в золото было заманчивой мечтой многих средневековых ученых. Интересно, что сегодня это превращение стало возможным с помощью ядерных реакций, однако искусственное золото оказывается намного дороже природного. Образец такого золота, полученный при облучении нейтронами изотопа ртути 196 Hg, хранится в Чикаго в Музее науки и промышленности. Алхимики удивились бы еще сильней, узнай они, что само золото в ядерных реакциях служит сырьем для получения изотопов франция и астата – элементов, которых практически нет в природе.
Золото представляет собой золотисто-желтый металл (tпл = 1064 о С), настолько мягкий и пластичный, что легко раскатывается в тончайшую фольгу, которую можно растереть в порошок. «Золото через свой изрядно жёлтый цвет и блещущую светлость от прочих металлов отлично», — писал о нем М.В.Ломоносов.
В природе золото встречается в виде мелких зёрен, перемешанных с песком или гравием – продуктами разрушения золотоносных пород. Правда, иногда находят и крупные самородки – массой несколько десятков килограммов.
Древние египтяне выделяли золото из золотоносных жил, пронизывающих кварцевые породы. Многократно раскаляя скалу в огне и обливая ее холодной водой, люди дробили камень, затем толкли его в ступах, мололи и лишь после этого промывали водой, раскладывая на наклонной плоскости. Отмытое золото сплавляли в слитки. Во времена Древнего Рима главным поставщиком золота была Испания, где его вымывали из земли, извлекаемой из рудников.

Добычу золота в Средние века подробно описал немецкий ученый Георг Агрикола. Золотоносную руду перемалывали в муку и перемешивали в специальных бочках, на дне которых находилась ртуть. Ртуть смачивала и частично растворяла золото с образованием амальгамы. Её отделяли от остальной породы и разлагали нагреванием. Ртуть при этом улетучивалась, а золото оставалось в перегонном аппарате.
С XIX в. для извдечения драгоценного металла стали применять цианистый метод: на воздухе золото взаимодействует с раствором цианида натрия, образуя комплексную соль – дицианоаурат (I) натрия:
а при обработке такого раствора цинком выделяется в свободном виде:
Сегодня золотоносными считаются породы с содержанием золота более 0,0001%. Ученые установили, что некоторые микроорганизмы способны поглощать золото. На этом открытии основан перспективный биохимический метод извлечения золота из отвальных пород.
Около половины производимого в мире золота используется в ювелирном деле. Ювелиры никогда не работают с чистым металлом, ведь он настолько мягок, что легко царапается и деформируется. Золото, содержащее примеси других металлов – меди, серебра, железа, — часто имеет тот или иной цветовой оттенок: от жёлтого и красновато-коричневого до розоватого или даже зеленоватого.
Благодаря высокой электропроводности и химической инертности золото активно используется в современной технике: тонким слоем этого металла покрывают контакты, электронагреватели, корпусы часов. На изготовление американского космического корабля «Колумбия» было израсходовано около 40 кг золота.
Еще одна область применения этого металла – медицина. В конце XIX в. немецкий микробиолог Роберт Кох обнаружил, что тетрацианоаурат (III) калия K[Au(CN)4] прекращает рост туберкулезных бактерий, а с 20-х гг. XX в. препараты золота, например санокризин Na3[Au(S2O3)2]∙2H2O, стали применять для лечения туберкулёза, артрита, а также в качестве противоспалительного средства.
Золото необычайно устойчиво к действию большинства окислителей: оно не реагирует с кислородом и не вытесняет водород из кислот. Однако говорить о полной инертности золота неверно: о его способности взаимодействовать с царской водкой знали уже алхимики. Наиболее традиционным методом окисления золота является обработка золотой фольги хлором в среде концентрированной соляной кислоты: 2Au + 3Cl2 + 2HCl = 2H[AuCl4]. Из образующейся при этом золотохлороводородной кислоты получают другие соединения золота. Все они легко могут быть восстановлены до металла.

Термин "металл" происходит от греческого слова "metalléuō", что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация по физическим свойствам
14. Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
13. Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы - это элементы с относительно высокой плотностью (обычно более 5 г/см³ ) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
12. Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы - это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
11. Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
10. Тугоплавкий металл
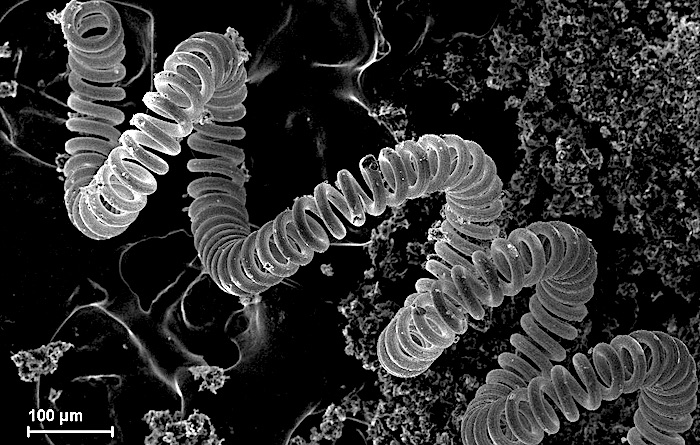
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
9. Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
Черные металлы: Сталь, чугун, сплавы железа.
Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин "железо" происходит от латинского слова "Ferrum", что переводится как «железо». Таким образом, термин «черный металл» обычно означает "содержащий железо", тогда как "цветной металл" означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
8. Цветные и благородные металлы

Ассортимент благородных металлов
Цветные металлы: медь, алюминий, олово, никель, цинк
Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы - это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель - для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
7. Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро - второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах.
Классификация по химическим свойствам
6. Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций.
Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов - использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
5. Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
4. Переходные металлы
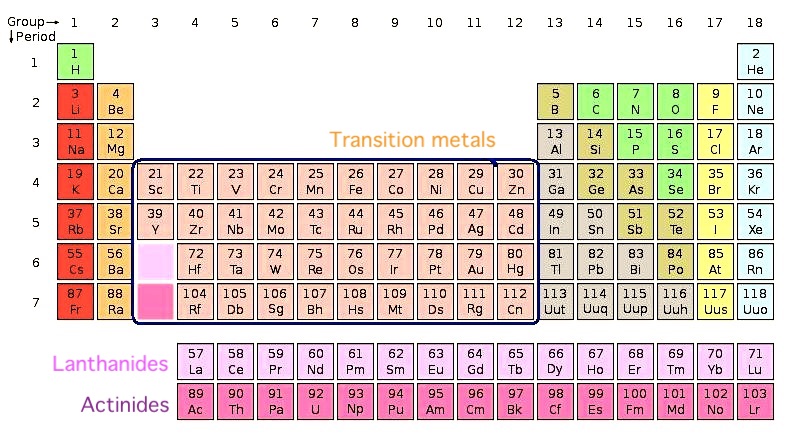
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
3. Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице - это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются "бедными" или "другими" металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий - в топливных элементах и полупроводниках.
2. Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды - это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды - это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
1. Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций
Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
МБОУ ВМР «Семенковская основная школа имени С.В.Солодягина»
« Металлы друзья и надежные помощники человека»
« Металлы друзья и надежные помощники человека»
Цель : 1. Углубить и расширить знания обучающихся о металлах (распространении в природе, истории открытия, физических свойствах, применении).
2. Показать связь теоретических знаний с их практическим использованием в жизни.
Оборудование :
Сплавы цветных металлов, чугун и сталь, плакаты с пословицами и поговорками о металлах, «черный ящик», волчок, реактивы соли - хлорид железа (2), хлорид железа(3) , гидроксид натрия, роданид калия, образец натрия, красная кровяная соль, пробирки
Правила : В игре участвуют 2 команды по 5 человек, остальные учащиеся болельщики каждой из команд. Есть капитаны, эмблема, название. Капитан крутит волчок, стрелка указывает номер вопроса. За правильный ответ команда получает 3 очка, за вопрос «черного ящика» 5 очков, за правильно проведенный опыт и объяснение результата команда получает 5 баллов. В «черном ящике» находится неизвестное вещество- металл, прочитав рассказ о нем, нужно определить его название.
Вступительное слово ведущего (название, цель, правила).
Представление команд (название, эмблема, приветствие).
Выступление учащегося:
Периодическая система химических элементов насчитывает в настоящее время 109 элементов, из них более 80 относятся к металлам. Значение их в жизни человека очень велико. Человек знал и применял металлы с древних времен. Раскопки археологов и изыскания историков подтверждают, что именно золото, серебро и медь были теми металлами, с которыми столкнулся человек на пути земной цивилизации.
В египетских гробницах, сооруженных за 1500 лет до н.э. найдена ртуть.
А металлургия золота, серебра, меди, свинца, олова, сурьмы была известна за 3000-4000 лет до н.э. Самые древние предметы из железа датированы 1300 г. до н.э. Железо в те времена ценилось во много раз дороже золота. В гробнице фараона Тутанхамона (14 в. до н.э.) найдено несколько предметов из железа: лезвия, амулет, кинжал.
В прошлом и до сего времени у некоторых народов и народностей кузнецы и металлурги считаются сродни богам, колдунам, волшебникам. В нашей стране уже 2,5 – 3 тысячелетия тому назад люди умели получать железо из руды и изготавливать из него оружие, орудия труда и предметы обихода. Однако первые железоделательные печи появились на Руси в 16-17вв. Выплавка составляла 150 тыс. пудов. При Петре 1 Урал становится ведущим горно - металлургическим районом. Выпуск чугуна в 1725 г. составил 19000т.
Причем русский металл был очень высокого качества.
А сейчас, учащиеся 2х команд проверят свои знания о металлах.
Вопросы викторины:
1. Алхимики утверждали: « Семь металлов создали свет по числу семи планет …» Назовите «эту» великолепную семерку? /золото, серебро, медь, железо, свинец, ртуть, олово/.
2. В каких географических названиях встречается медь? / Медногорск (г.на Южном Урале),о.Медный (один из Командорских островов), Кипр ( от лат.« купрум»).
3. Какой металл академик Ферсман назвал» металлом консервной банки?
Правомерно ли это определение в наше время? / Олово./ До сих пор в консервную промышленность, использовавшую банки из жести, покрытой оловом, идет значительная часть этого металла. В условиях растущего оловянного дефицита в последние годы вместо белой жести применяется безоловянная жесть с хромовым покрытием, а в будущем основным «металлом консервной банки» станет алюминий.
4. Если бы существовал приз «за активность», то атомам, какого из металлов вы бы его присудили? / Цезию, если не считать франция, которого практически нет в природе/.
5 . « Черный ящик» Это металл древнейших цивилизаций. Он служит более 8 тыс. лет. Это тяжелый металл ( P = 11,34 г/см), темно- серого цвета, покрытый с поверхности синевато- серой оксидной пленкой. Он относительно мягок, его можно прокатывать в тонкие листы. Это свойство использовалось в глубокой древности при изготовлении труб для древнеримского водопровода. Трубы первого российского трубопровода, построенного в 1633 г. для обслуживания Московского Кремля, также были изготовлены из него.
Качество воды в результате резко ухудшилось: концентрация этого металла в воде в 833 раза превышала современные предельно допустимые нормы.
В настоящее время использование этого металла в быту резко сократилось.
Основная область применения этого металла - изготовление сплавов. Дайте
название этому металлу ?/ Свинец/.
6.Если верить древнему историку, то во времена похода Александра Македонского в Индию офицеры его армии болели желудочно-кишечными заболеваниями гораздо реже, чем солдаты. Еда и питье у них были одинаковыми, а вот металлическая посуда разная. Из какого чудодейственного металла была сделана посуда офицеров? / Серебро-бактерицидные свойства/.
7.Назовите самый твердый из металлов (режет стекло)? / Хром/
8.Почему морскую воду можно назвать «жидкой железной рудой»? / Если извлечь все железо, растворенное в морской воде, то его придется по 35 т на
каждого жителя планеты, в то время как за все существование человечества произведено по 6 т на каждого ныне живущего человека.
9.Назовите самый легкий металл, его плотность? / Литий, 0,53 г/ см).
10.Назовите самый распространенный металл в земной коре? / Алюминий/
11. Опыт. Предложите способ определения следующих солей – хлорид железа (2), хлорид железа(3), проведите определение? Объясните результаты.
12. Какие металлы обладают магнитными свойствами ?/ Железо, никель, кобольт/.
13.Назовите самый тугоплавкий металл, его температура плавления? /Вольфрам, t - 3390 C /
14. Какой химический элемент изображали в 17 в. в виде воина? / Железо/
15 . « Черный ящик». В виде порошкообразного вещества этот металл был впервые получен в 1827г. немецким ученым Фридрихом Велером. Очень сложной оказалась задача получения его в виде слитка. 18 лет упорного труда позволили исследователю приготовить его в виде маленьких, размером с булавочную головку гранул. Новый металл оказался красивым, похожим на серебро, но значительно более легким. Эти ценные качества определили его стоимость: в конце 19- начале 20в. он ценился выше золота. После того как, нашли технологии его получения в больших количествах, он быстро подешевел и приобрел широкую популярность. В нашей стране был впервые получен 14 мая 1932 г. в слитках серебристого цвета на Волховском комбинате. О каком металле идет речь? / Алюминий/
16. Опыт. Проделайте качественную реакцию на ион железа 3+. Для этого к раствору хлорида железа(3) прилейте несколько капель роданида калия. Что наблюдаете? Напишите уравнения реакций в молекулярном и ионном виде.
17.Встречается ли на Земле чистое железо, если да, то в виде чего? /Да, в виде метеоритов/.
18.Назовите самые легкоплавкие металлы, их температуры плавления? /Цезий, t =28,4 C ,ртуть , t =38,9 C /
19.Назовите три металла - лучшие проводники электрического тока? /Серебро, медь, алюминий/
20.Перечислите области применения алюминия? Какие сплавы алюминия вы знаете? Их состав? / Силумин - алюминий – 75 %, кремний -25 %; магналин алюминий – 85%, магний – 15% ; дуралюмин алюминий – 90 %, медь – 8%, сера, магний, марганец, железо -2% /
21. Чем нельзя потушить горящий калий: песком, водой, огнетушителем? Почему? / Водой/
22. Какой металл называют металлом неутомимости, т.к. он способен выдерживать высокие нагрузки. Он и его сплавы применяются для изготовления теплозащитных конструкций космических кораблей, в атомных реакторах, радиоэлектронике. Но для широкого применения он не пригоден, т.к. ядовит, дорог, хрупок? / Бериллий/.
23. Назовите несколько металлов, используемых в гальваностегии- нанесении путем электролиза на поверхность металлических изделий слоев других металлов, с целью предохранения их от коррозии? / Никель, хром, свинец, олово, цинк/.
24. Назовите металл, входящий в состав латуни? / Цинк/.
25 . « Черный ящик». Этот металл встречается на Земле повсеместно, на его долю приходится 4,5 % атомов земной коры. Оно есть почти во всех глинах, песках, горных породах. В некоторых местах оно образует скопления руд.
Организм взрослого человека содержит около 3 г его. Но это все - в связанном виде. Чистый металл на Земле имеет преимущественно космическое происхождение. Ценные качества этого металла побудили человека еще во 2 тысячелетии до н.э. направить огромные усилия на нахождение способов его получения (восстановления) из руд. Назовите металл? / Железо/.
26. Какой металл, широко применяемый сейчас, несколько десятилетий тому назад считался драгоценным ?/Алюминий/.
27.Какие элементы металлы носят названия планет? / Уран, Нептуний, Плутоний /.
28.Перечислите области применения железа? Что такое чугун, сталь?
29.Что обозначает выражение « Металл, принесенный в жертву рыжему дьяволу? / Железо, превращенное в ржавчину - коррозия /.
30. Атомы, каких химических элементов металлов входят в состав марганцовки?
/ Калий, марганец/.
31. Какой из металлов в глубокой древности называли «небесной медью» и почему? / Железо метеоритов, обрабатывали также, как и медь/.
32.О каком металле говорят: « В грамм добыча, в год труды»? / Радий/.
33. Опыт. Проделайте качественную реакцию на ион железа 2+. Для этого к раствору хлорида железа(2) прилейте несколько капель красной кровяной соли. Что наблюдаете? Напишите уравнения реакций в молекулярном и ионном виде.
34. Латинское название серебра, золота? «Аргентум», « Аурум».
35. « Черный ящик». Металл достаточно мягкий, пластичный. Имеет температуру плавления 1083 С. Отличный проводник электрического тока (после серебра). Биологическая роль- катализатор внутриклеточных окислительных процессов. Соединения этого металла используются для борьбы с вредителями с/х культур. Цвет - светло- розовый. Широко применяется в электротехнической промышленности, для изготовления сплавов. Название металла? / Медь/.
36. Какой металл называют автомобильным? / Ванадий/
37.Назовите единственный металл, находящийся при обычных условиях в жидком состоянии? / Ртуть/.
38.Назовите самый тяжелый металл, его плотность? / Осмий, P = 22,6 г/ см /
39. Как хранят металлический натрий? Почему? /образец металла /
40. Когда в 1855 году на Парижской выставке был выставлен алюминиевый слиток, на него смотрели как на редчайшую драгоценность. Чем это можно объяснить?
41.Железный купорос, применяющийся в производстве чернил и красок, при окрашивании тканей, получают растворением обрезков стали в растворе серной кислоты. Составьте соответствующее уравнение реакции.
42. При выплавлении меди и бронз нередко приходится иметь дело с нежелательными примесями (водород, азот и др.). Как вы думаете, зачем в расплав добавляют стронций?
Подведение итогов : подсчет набранных баллов.
Конкурс болельщиков :
Придумать пословицы и поговорки о металлах.(за поговорку 2 балла)
« Слово- серебро, молчание- золото».
«Не все то золото, что блестит».
«В народе без железа, как при обеде без соли».
«Если ты настоящий человек, будь крепким, как сталь».
«Правдивое слово и железо пробьет».
«Пока железо в работе, его ржа не берет».
Конкурс « Разгадай чайнворд « Металлы»» .
Химические знаки металлов в центре спирали - ключ к решению чайнворда. Расположите в клетках спирали названия девяти указанных металлов.
Заключительное слово, обобщение.
Читайте также:

